
A.Mn、Fe均为第四周期过渡元素,两元素的部分电离能(I)数据列于下表:
元素 | Mn | Fe | |
电离能/kJ·mol-1 | I1 | 717 | 759 |
I2 | 1 509 | 1 561 | |
I3 | 3 248 | 2 957 | |
回答下列问题:
(1)Mn元素价电子层的电子排布式为_____________,比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难。对此,你的解释是____________________。
(2)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物,则与Fe原子或离子形成配合物的分子或离子应具备的条件是________________________。
(3)三氯化铁常温下为固体,熔点
(4)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如下图所示。面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为____________。

B.有机化合物A的分子式是C13H20O8(相对分子质量为304),1 mol A在酸性条件下水解得到4 mol CH3COOH和1 mol B。B分子结构中每一个连有羟基的碳原子上还连有两个氢原子。
请回答下列问题:
(1)A和B的相对分子质量之差是____________。
(2)B的结构简式是_________________。
(3)B能发生的反应是___________(填写序号)。
①氧化反应 ②取代反应 ③消去反应 ④缩聚反应
(4)已知:

以两种一元醛(其物质的量之比为1∶4)和必要的无机试剂为原料合成B,写出合成B的各步反应的化学方程式。
A.(1)3d54s2 由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态(或Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态)
(2)具有孤对电子 (3)分子 (4)2∶1
解析:(2)可以利用教材知识直接得出,(3)是利用晶体性质对晶体类型的判定,比较简单;(4)是对晶体中原子分摊的考查,在面心立方中,铁原子数为8×1/8+6×1/2=4个,体心立方中铁原子数为8×1/8+1=2个,所以个数比为2∶1。
B.(1)168 (2)C(CH2OH)4
(3)①②④
(4)CH3CHO+3HCHO![]() (CH2OH)3CCHO
(CH2OH)3CCHO
(CH2OH)3CCHO+HCHO+NaOH(浓)![]() C(CH2OH)4+HCOONa
C(CH2OH)4+HCOONa
解析:在解析时要注意,1 mol A在酸性条件下水解得到4 mol乙酸和1 mol B,则B分子中含有4个羟基,又因为B分子结构中每一个连有羟基的碳原子上还连有两个氢原子,不难得出B的结构,从而顺利得出(1)(2)(3)的答案;(4)题中可以利用信息,得出两种醛分别为乙醛和甲醛,然后得出答案。


科目:高中化学 来源: 题型:阅读理解
《物质结构与性质》模块选择题
1.下列性质不能用金属键理论解释的是
A.导电性 B.导热性 C.延展性 D.锈蚀性
2.下列说法错误的是
A.O3与SO2的结构与性质相似
B.硫粉不溶于水,易溶于CS2中
C.Be(OH)2是两性氢氧化物
D.在相同条件下, 的沸点高于
的沸点高于![]()
3.氨气溶于水时,大部分NH3与H2O以氢键(用“…”表示)结合形成NH3·H2O分子,根据氨水的性质可推知NH3·H2O的结构式为
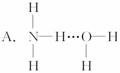

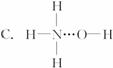

《有机化学基础》模块选择题
4.已知某有机物A的分子式C2H6O的红外光谱和核磁共振氢谱如下图所示,下列说法中错误的是
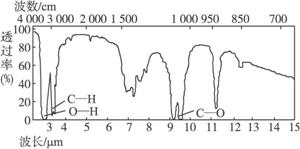
未知物A的红外光谱
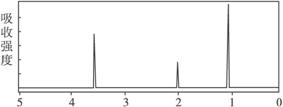
未知物A的核磁共振氢谱
A.由红外光谱可知,该有机物中至少含有三种不同的化学键
B.由核磁共振氢谱可知,该有机物分子中有三种不同的氢原子且个数比为1∶2∶3
C.仅由其核磁共振氢谱可知其分子中的各类型氢原子总数
D.则A的结构简式为CH3—O—CH3
5.在阿司匹林的结构简式(下式)中①②③④⑤⑥分别标出了其分子中的不同的键。将阿司匹林与足量NaOH溶液共煮时,发生反应时断键的位置是
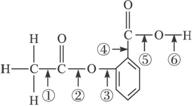
A.①④ B.②⑤ C.③④ D.②⑥
6.举办“人文奥运”的一个重要体现就是禁止运动员服用兴奋剂。有一种兴奋剂的结构简式如下式,下列有关该物质的说法正确的是
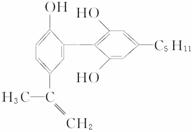
A.该分子中所有碳原子可以稳定地共存在一个平面中
B.1 mol该物质与浓溴水和H2反应时,最多消耗Br2和H2的物质的量分别为4 mol、7 mol
C.遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物
D.滴入酸性KMnO4溶液,观察到紫色褪去,可证明分子中存在双键
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
《有机化学基础》模块试题
1.有机黏合剂的黏合过程是液态的小分子黏合剂经化学反应转化为大分子或高分子而固化。
(1)“502胶”是一种快干胶,其主要成分为α氰基丙烯酸乙酯( ),请写出“502胶”发生黏合作用的化学方程式:_____________________________;反应类型是_____________。
),请写出“502胶”发生黏合作用的化学方程式:_____________________________;反应类型是_____________。
(2)厌氧胶( )也是一种黏合剂,工业上用丙烯酸和某物质在一定条件下反应可制得这种黏合剂,该物质的名称是_____________;请写出这一制取过程的化学方程式_________________。
)也是一种黏合剂,工业上用丙烯酸和某物质在一定条件下反应可制得这种黏合剂,该物质的名称是_____________;请写出这一制取过程的化学方程式_________________。
(3)白乳胶是常用的黏合剂,其主要成分为醋酸乙烯酯(CH3COOCH=CH2),它有多种同分异构体,如 、
、 、
、 。已知含有
。已知含有![]() 结构的物质不能稳定存在。请另外写出3种含—CH=CH—结构的链状同分异构体的结构简式:______________、______________、______________。
结构的物质不能稳定存在。请另外写出3种含—CH=CH—结构的链状同分异构体的结构简式:______________、______________、______________。
(4)已知醇和醛可以发生反应:2CH3OH+HCHO![]() CH3OCH2OCH3+H2O,聚乙烯醇可用做普通胶水,它的羟基可全部与丁醛(CH3CH2CH2CHO)缩合脱水,得到含六原子环的强力黏合剂聚乙烯缩丁醛。请写出制取聚乙烯缩丁醛的化学方程式:________________。
CH3OCH2OCH3+H2O,聚乙烯醇可用做普通胶水,它的羟基可全部与丁醛(CH3CH2CH2CHO)缩合脱水,得到含六原子环的强力黏合剂聚乙烯缩丁醛。请写出制取聚乙烯缩丁醛的化学方程式:________________。
《物质结构与性质》模块试题2.如下图是Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。

(1)请写出上图中d单质对应元素原子基态时的电子排布式_____________。
(2)单质a、f、b对应的元素以原子个数比1∶1∶1形成的分子中含_____________个σ键,_____________个π键。
(3)a与b的元素形成的10电子中性分子X的空间构型为_____________;将X溶于水后的溶液滴入到含d元素高价离子的溶液中至过量,生成的含d元素离子的化学式为________
_______,其中X与d的高价离子之间以_____________键结合。
(4)上述六种元素中的一种元素形成的含氧酸的结构为:![]() ,该含氧酸的分子式为_____________,请简要说明该物质易溶于水的原因__________________________。
,该含氧酸的分子式为_____________,请简要说明该物质易溶于水的原因__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com