
��11�֣���֪NaHCO3����ʱ�ܽ��С����°��Ƽ�ķ����ǣ����ı���ʳ��ˮ��ͨ������Ķ�����̼�����о��������������ˡ�ϴ�ӡ����յô���˹��̿��Ա�ʾΪ��
�� NaCl (����) + NH3+CO2+H2O��NaHCO3��+NH4Cl���˷�Ӧ�Ƿ��ȷ�Ӧ��
�� 2NaHCO3 Na2CO3 +CO2��+H2O
Na2CO3 +CO2��+H2O
��ij��ѧС���������ԭ����ʵ������ģ���Ƽ���̣���ͼCװ�������а���NaCl����Һ���Ҷ��߾��ﵽ�˱��͡�
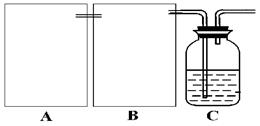
��1����CO2ʱΪ��ʹ��Ӧ�濪���ã������ͣ����ͼA������Ӧѡ������ װ�ã�����ţ���������װ���������ͣ������ ��
��2��Ϊʹʵ���ܹ����У���B��������Ӧѡ����ͼ�е� װ�ã���д��ţ�����װ����Ӧװ����Լ��� ��
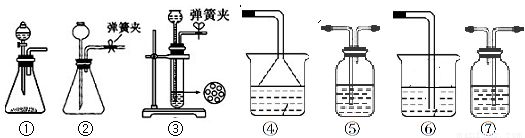
��3����С��ͬѧ����ȷ�ķ�������װ�ã����������Ժϸ�����ʵ�飬���������ľ���dz��٣�����ʦ��ָ���£����Ƕ�ij��װ�ý����˸Ľ����ﵽ��ʵ��Ŀ�ġ�����Ϊ���ǵĸĽ������� ��
��4�������ñ���ʳ��ˮ�к���NaCl������Ϊ5.85g��ʵ���õ������NaHCO3���������Ϊ5.46g������ڶ����ֽ�ʱû����ʧ����Na2CO3�IJ���Ϊ (����Ϊʵ�ʲ���ռ���۲����İٷֱ�)��
��1���ۣ�1�֣����رյ��ɼк�Ӧ���ɵ�����ʹ�ϲ�ѹǿ������һ���̶Ⱥ�ɰѷ�ӦҺѹ��©����ʹ��Һ����Ӷ�ֹͣ��Ӧ ��2�֣�
��2���ݣ�1�֣� ����̼��������Һ ��1�֣�
��3����Cװ�ý�����һ��ʢ�б�ˮ������ˮ�������ձ��У���2�֣�
��4��65%��2�֣�
��������
�����������1�����ܿ��Ʒ�Ӧ�ķ�������Ӧ��ֹͣ�����룬�ڲ��ܿ��Ʒ�Ӧ�ķ�����ֹͣ��ֻ�Т�ͨ��ֹˮ�������Ʒ�Ӧ�ķ�����ֹͣ���رյ��ɼк�Ӧ���ɵ�����ʹ�ϲ�ѹǿ������һ���̶Ⱥ�ɰѷ�ӦҺѹ��©����ʹ��Һ����Ӷ�ֹͣ��Ӧ��
��2��Bװ�õ������dz�ȥ������̼�л��е��Ȼ������壬�ʲ��ý�����ͨ��װ����̼��������Һ��ϴ��ƿ�����Ȼ��⡣��ѡ��ݡ�
��3��Ϊ���Ӿ�����������ɲ�ȡ����ʹ̼�����Ƶ��ܽ�ȼ�С�Ӷ������������ʸĽ���������Ϊ����Cװ�ý�����һ��ʢ�б�ˮ������ˮ�������ձ��У�����
��4��������ԭ���غ�2NaCl-------Na2CO3
117 �� 106
5.85 �� 5.3
���ۿ�����Na2CO3Ϊ5.3�ˣ�
����Ϊ
2NaHCO3 -------Na2CO3
168g �� 106g
5.46g �� 3.45g
ʵ�ʵõ�̼����Ϊ3.445��
����Na2CO3�IJ�����3.445/5.3=0.65
���㣺�������ȡ
��������������Ƽ��ԭ����������ע�����=ʵ������/���۵õ���������


 �߽�������ϵ�д�
�߽�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ||

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��15�֣���֪NaHCO3����ʱ�ܽ��С����°��Ƽ�ķ����ǣ����ı���ʳ��ˮ��ͨ������Ķ�����̼�����о��������������ˡ�ϴ�ӡ����յô���˹��̿��Ա�ʾΪ��
�� NaCl (����) + NH3+CO2+H2O��NaHCO3��+NH4Cl���˷�Ӧ�Ƿ��ȷ�Ӧ��
�� 2NaHCO3 Na2CO3+CO2��+H2O
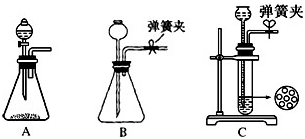
��ij��ѧС���������ԭ����ʵ������ģ���Ƽ���̣���ͼCװ�������а���NaCl����Һ���Ҷ��߾��ﵽ�˱��͡�
��1����CO2ʱΪ��ʹ��Ӧ�濪���ã������ͣ����ͼA������Ӧѡ������ װ�ã�����ţ���������װ���������ͣ������ ��
��2��Ϊʹʵ���ܹ����У���B��D�����ڲ�������װ�ã� ����װ��ͼ���ڴ���ϣ�����ָ�������Լ��� ��
��3����С��ͬѧ����ȷ�ķ�������װ�ã����������Ժϸ�����ʵ�飬���������ľ���dz��٣�����ʦ��ָ���£����Ƕ�ij��װ�ý����˸Ľ����ﵽ��ʵ��Ŀ�ġ�����Ϊ���ǵĸĽ������� ��
��4�������ñ���ʳ��ˮ�к���NaCl������Ϊ5.85g��ʵ���õ������NaHCO3���������Ϊ5.46g������ڶ����ֽ�ʱû����ʧ����Na2CO3�IJ���Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�����ʡƽ��ɽ�и�һ��ѧ����ĩ���п��Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
��15�֣���֪NaHCO3����ʱ�ܽ��С����°��Ƽ�ķ����ǣ����ı���ʳ��ˮ��ͨ������Ķ�����̼�����о��������������ˡ�ϴ�ӡ����յô���˹��̿��Ա�ʾΪ��
�� NaCl (����) + NH3+CO2+H2O��NaHCO3��+NH4Cl���˷�Ӧ�Ƿ��ȷ�Ӧ��
�� 2NaHCO3  Na2CO3 +CO2��+H2O
Na2CO3 +CO2��+H2O
��ij��ѧС���������ԭ����ʵ������ģ���Ƽ���̣���ͼCװ�������а���NaCl����Һ���Ҷ��߾��ﵽ�˱��͡�
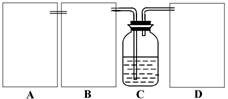
��1����CO2ʱΪ��ʹ��Ӧ�濪���ã������ͣ����ͼA������Ӧѡ������ װ�ã�����ţ���������װ���������ͣ������ ��
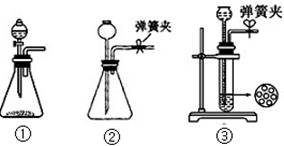
��2��Ϊʹʵ���ܹ����У���B��D�����ڲ�������װ�ã� ����װ��ͼ���ڴ���ϣ�����ָ�������Լ��� ��
��3����С��ͬѧ����ȷ�ķ�������װ�ã����������Ժϸ�����ʵ�飬���������ľ���dz��٣�����ʦ��ָ���£����Ƕ�ij��װ�ý����˸Ľ����ﵽ��ʵ��Ŀ�ġ�����Ϊ���ǵĸĽ������� ��
��4�������ñ���ʳ��ˮ�к���NaCl������Ϊ5.85g��ʵ���õ������NaHCO3���������Ϊ5.46g������ڶ����ֽ�ʱû����ʧ����Na2CO3�IJ���Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��ɽ��ʡ�����и�һ��ѧ����ĩģ�⻯ѧ�Ծ� ���ͣ�ʵ����
��15�֣���֪NaHCO3����ʱ�ܽ��С����°��Ƽ�ķ����ǣ����ı���ʳ��ˮ��ͨ������Ķ�����̼�����о��������������ˡ�ϴ�ӡ����յô���˹��̿��Ա�ʾΪ��
�� NaCl (����) + NH3+CO2+H2O��NaHCO3��+NH4Cl���˷�Ӧ�Ƿ��ȷ�Ӧ��
�� 2NaHCO3  Na2CO3
+CO2��+H2O
Na2CO3
+CO2��+H2O
��ij��ѧС���������ԭ����ʵ������ģ���Ƽ���̣���ͼCװ�������а���NaCl����Һ���Ҷ��߾��ﵽ�˱��͡�

��1����CO2ʱΪ��ʹ��Ӧ�濪���ã������ͣ����ͼA������Ӧѡ������ װ�ã�����ţ���������װ���������ͣ������ ��

��2��Ϊʹʵ���ܹ����У���B��D�����ڲ�������װ�ã� ����װ��ͼ���ڴ���ϣ�����ָ�������Լ��� ��
��3����С��ͬѧ����ȷ�ķ�������װ�ã����������Ժϸ�����ʵ�飬���������ľ���dz��٣�����ʦ��ָ���£����Ƕ�ij��װ�ý����˸Ľ����ﵽ��ʵ��Ŀ�ġ�����Ϊ���ǵĸĽ������� ��
��4�������ñ���ʳ��ˮ�к���NaCl������Ϊ5.85g��ʵ���õ������NaHCO3���������Ϊ5.46g������ڶ����ֽ�ʱû����ʧ����Na2CO3�IJ���Ϊ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com