
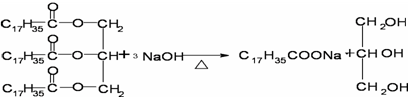
 ;向混合液中加入食盐使高级脂肪酸钠的溶解度降低而析出,然后过滤即可,故答案为:
;向混合液中加入食盐使高级脂肪酸钠的溶解度降低而析出,然后过滤即可,故答案为: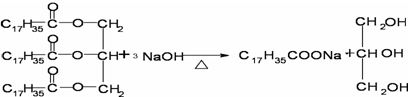 ;D;
;D;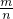 ,始终是一个不变量,所以容器内气体的平均相对分子质量不变时,不一定是平衡状态,故C错误;
,始终是一个不变量,所以容器内气体的平均相对分子质量不变时,不一定是平衡状态,故C错误;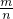 ;
;

科目:高中化学 来源: 题型:
 +3NaOH→3C17H35COONa+
+3NaOH→3C17H35COONa+
 +3NaOH→3C17H35COONa+
+3NaOH→3C17H35COONa+
查看答案和解析>>
科目:高中化学 来源: 题型:
 +3NaOH→3C17H35COONa+
+3NaOH→3C17H35COONa+
 +3NaOH→3C17H35COONa+
+3NaOH→3C17H35COONa+
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图为硬脂酸甘油脂在碱性条件下水解的装置图.进行皂化反应的步骤如下:
如图为硬脂酸甘油脂在碱性条件下水解的装置图.进行皂化反应的步骤如下:| △ |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
高中阶段常用化学反应方程式
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com