
下列关于0.2mol/L的Fe2(SO4)3溶液的正确说法是
A.500mL溶液中含SO42-、Fe3+总数为NA
B.500mL溶液中含0.6NA个SO42-
C.1L溶液中含有0.2NA个Fe3+
D.500mL溶液中SO42-物质的量浓度为0.6mol/L
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2014-2015学年山东安丘市期中考试高二化学模拟(A)卷(解析版) 题型:选择题
在298K时,2SO2(g)+O2(g)  2SO3(g) ΔH=-197 kJ·mol-1 ,在相同的温度下,向密闭真空容器中通入2molSO2和1molO2,达到平衡时放出热量Q1; 向另一个同体积的密闭真空容器中通入1molSO2和0.5molO2,达到平衡时放出热量Q2,则下列关系中正确的是:( )
2SO3(g) ΔH=-197 kJ·mol-1 ,在相同的温度下,向密闭真空容器中通入2molSO2和1molO2,达到平衡时放出热量Q1; 向另一个同体积的密闭真空容器中通入1molSO2和0.5molO2,达到平衡时放出热量Q2,则下列关系中正确的是:( )
A.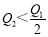 B.
B. C.
C.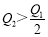 D.
D.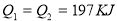
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省江淮十校高三8月联考化学试卷(解析版) 题型:选择题
某化学科研小组研究合成氨:N2(g)+3H2(g)  2NH3(g);△H<0,在其他条件不变时,改变某一条件时对化学平衡的影响,得到如下图像,以下对应选项中正确的是( )
2NH3(g);△H<0,在其他条件不变时,改变某一条件时对化学平衡的影响,得到如下图像,以下对应选项中正确的是( )
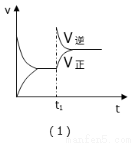

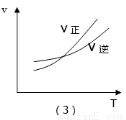
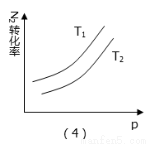
A.(1)对应的是:在t1时恒压条件下,通入NH3,
B.(2)对应的是:氨气在恒容不同温度下的百分含量
C.(3)对应的是:在恒容条件下,反应速率与温度的关系
D.(4)对应的是:N2转化率与温度(T1>T2)、压强的关系
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏高一上学期第一次月考化学试卷(解析版) 题型:选择题
某气体的质量是9.5g,体积是5.6升(标准状况下),该气体的摩尔质量是
A.38 B.38g·mol-1 C.19 D.19g·mol-1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏高一上学期第一次月考化学试卷(解析版) 题型:选择题
容量瓶上需标有以下六项中的
①温度②浓度③容量④压强⑤刻度线⑥酸式或碱式
A.①③⑤ B.③⑤⑥ C.①②④ D.②④⑥
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏高一上学期第一次月考化学试卷(解析版) 题型:选择题
一般检验SO42-的试剂是
A、BaCl2 、稀HNO3 B、AgNO3 、稀HNO3 C、 稀HCl BaCl2 D、AgNO3 稀HCl
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市和平区高二上学期期中考试化学试卷(解析版) 题型:填空题
(11分)(1)某恒温恒容容条件下的可逆反应: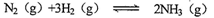 △H<O,起始充入amol N2 、bmol H2,达到平衡后,N2、H2、NH3的物质的量分别为1 mol、3 mol、10 moL,回答下列问题:
△H<O,起始充入amol N2 、bmol H2,达到平衡后,N2、H2、NH3的物质的量分别为1 mol、3 mol、10 moL,回答下列问题:
①a=___________,b=___________。
②平衡后,再充入5 mol NH3,化学平衡将向__________移动(填“左”或“右”或“不移动”),再达新平衡时N2的百分含量_______(填“>”、“<”、“=”)原平衡时N2的百分含量;
③平衡后若升高温度,则平衡向________(填“向左”或“向右”)方向移动;若增加压强,则平衡向________(填“向左”或“向右”)方向移动。
(2)某恒温恒压条件下的可逆反应: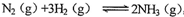 ,起始充入1 mol N2、
,起始充入1 mol N2、
3 molH2 、16 mol NH3,容器的容积为VL。达到平衡后,N2、H2、NH3的物质的量分别为amol、b mol、cmol,此时容器的容积为.1VL,回答下列问题:
①起始时反应速率v(正)____(填“>”、“<”、“=”)v(逆)。
②平衡时a=________,b=_______。
③若平衡后再充入3.6 mol NH3,重新建立平衡时容器的容积为_____________L。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市和平区高二上学期期中考试化学试卷(解析版) 题型:选择题
在101 kPa和25℃时,有反应的热化学方程式:
H2(g) + 1/2O2(g) =H2O(g) △H=-241.8kJ/mol,
H2(g) + 1/2O2(g) =H2O(1) △H=-285.8kJ/mol下列说法中错误的是
A.H2燃烧生成1mol H2O (g)时,放出241.8 kJ的热量
B.H2的燃烧热为-285.8 kJ
C.O2前面的1/2表示参加反应的O2的物质的量
D.1 mol液态水变成水蒸气时吸收44 kJ的热量
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川邛崃市高二上学期第一次月考化学试卷(解析版) 题型:选择题
下表中元素均为中学化学常见短周期元素根据表中信息,下列说法不正确的是
元素代号 | X | Y | Z | W | N |
原子半径/nm | 0.186 | 0.074 | 0.102 | 0.099 | 0.16 |
主要化合价 | +1 | -2 | -2+6 | +7-1 | +2 |
A.X和W形成的化合物是共价化合物
B.常温下单质与水反应速率X大于N
C.最高价氧化物对应水化物酸性W大于Z
D.X和Y的单质在一定条件下反应可生成一种淡黄色的固体化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com