
【题目】某同学拟用含少量Fe2O3杂质的废铜粉制备无水硫酸铜,设计了如下流程:
下列有关说法不正确的是( )
A.“过量酸”不适合用硝酸或浓硫酸,固体B可以用CuO、Cu(OH)2或Cu2(OH)2CO3
B.通入的气体A可以是O2或Cl2
C.通入气体A之前的混合溶液中存在的阳离子是:Fe2+、Cu2+、H+
D.将从溶液中得到的硫酸铜晶体在空气中加热,可制得无水硫酸铜
【答案】B
【解析】解:A、为了制得硫酸铜,废铜粉应与稀硫酸反应,所以“过量酸”为稀硫酸,若用浓硫酸,则Cu与浓硫酸反应生成SO2气体造成空气污染,若用浓硝酸,则发生反应Cu + 4HNO3 = Cu(NO3)2 + 2NO2↑+2H2O,一方面产生污染性气体NO2 , 另一方面混入Cu(NO3)2杂质;加入固体B的作用是调节溶液的pH,使Fe3+转化为沉淀而除去,为了不引入新的杂质,可选用CuO、Cu(OH)2或Cu2(OH)2CO3与过量的酸反应生成硫酸铜,A正确。B、通入气体A的目的是将Fe2+氧化为Fe3+ , 所以气体A可以是氧气,但不能是氯气,以免引入氯化铁杂质,B不正确。C.废铜粉与稀硫酸的反应Fe2O3 + 6H+ = 2 Fe3+ + 3H2O、2Fe3+ +Cu==2 Fe2++Cu2+由于铜过量,则溶液中不含Fe3+ , 又因稀硫酸过量,则溶液中合有H+ , 因此通入气体A之前的混合溶液中存在的阳离子是:- Fe2+、Cu2+、H+ , C正确。D.硫酸铜晶体在空气中加热,失去结晶水可制得无水硫酸铜,D正确。


科目:高中化学 来源: 题型:
【题目】按照物质的树状分类和交叉分类,H2SO4应属于( )
①酸 ②氧化物 ③含氧酸 ④二元酸 ⑤纯净物 ⑥混合物 ⑦无机化合物
A. ①③④⑤⑦
B. ①②③④⑤⑦
C. ①②③④⑥
D. ①④⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度一定时,在密闭容器中发生可逆反应:mA(s)+nB(g)pC(g),达到平衡后,若将混合气体的体积压缩到原来的 ![]() ,当再次达到平衡时,C的浓度为原平衡时C的浓度的1.9倍,则下列叙述中正确的是( )
,当再次达到平衡时,C的浓度为原平衡时C的浓度的1.9倍,则下列叙述中正确的是( )
A.m+n<p
B.C气体的体积分数增大
C.平衡向正反应方向移动
D.B的转化率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】世界卫生组织(WHO)将二氧化氯(ClO2)列为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有着广泛应用,由此可判断二氧化氯()。
A.是强氧化剂
B.是强还原剂
C.是离子化合物
D.分子中氯为负1价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列示意图与对应的反应情况符合的是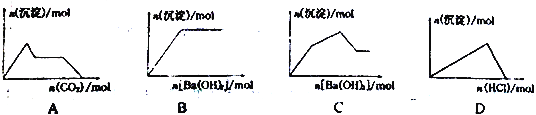
A. 向含0.01molKOH和0.01mo1Ca(OH)2的混合溶液中缓慢通入CO2至过量
B. 向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量
C. 向KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液至过量
D. 向NaAlO2溶液中逐滴加入盐酸至过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某试剂瓶上贴有如下标签,对该试剂理解正确的是
![]()
A. 该溶液中含有的微粒主要有:NaCl、Na+、Cl-、H2O
B. 若取50毫升溶液,其中的c(Cl-)=0.05 mol/L
C. 若取该溶液与0.1 mol/L AgNO3 100 mL溶液完全反应,需要取该溶液10 mL
D. 该溶液与1.0mol/LNa2SO4溶液的c(Na+)相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com