
| A. | ①④②③ | B. | ④①②③ | C. | ②④①③ | D. | ④②①③ |
分析 粗盐样品含有Ca2+、Mg2+、SO42-及泥砂,除去钙离子用碳酸钠,除去镁离子用氢氧根离子,除去硫酸根离子用钡离子,由于加入的试剂均过量,则加入碳酸钠溶液应该放在氢氧化钡溶液之后,然后过滤除去泥沙和沉淀,最后加入盐酸除去过量的氢氧根离子、碳酸根离子即可,据此进行解答.
解答 解:粗盐样品含有Ca2+、Mg2+、SO42-及泥砂,除去Ca2+用过量的NaCO3溶液,除去Mg2+用氢氧根离子,除去SO42-用钡离子,由于加入的试剂均过量,则加入NaCO3溶液应该放在氢氧化钡溶液之后,然后过滤除去泥沙和沉淀,最后加入盐酸除去过量的氢氧根离子、碳酸根离子,
根据分析可知,④必须放在②之后,所以选项中正确只有②④①③,
故选C.
点评 本题考查了粗盐的提纯,题目难度不大,明确加入试剂及先后顺序为解答关键,试题侧重基础知识的考查,有利于提高学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| A. | 升高温度,气体颜色加深,则此反应为吸热反应 | |
| B. | 慢慢压缩气体体积,平衡向正反应方向移动,混合气体的颜色变浅 | |
| C. | 慢慢压缩气体体积,若体积减小一半,压强增大,但小于原来的两倍 | |
| D. | 恒温恒容时,充入惰性气体,压强增大,平衡向正反应方向移动,混合气体的颜色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③①② | B. | ②①③ | C. | ①②③ | D. | ②③① |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
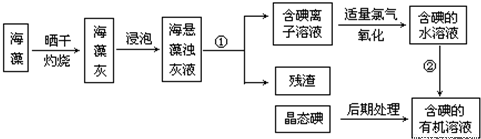
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
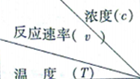 | 1.200 | 1.000 | 0.800 | 0.600 |
| 270 | 3.60 | 3.00 | 2.40 | 1.80 |
| 280 | 9.00 | 7.50 | a | 4.50 |
| b | 2.16 | 1.80 | 1.44 | 1.08 |
| A. | 升高温度或增大A的浓度都可以增大v的值 | |
| B. | 同时改变反应温度和A的浓度,v可能不变 | |
| C. | a=6.00 | |
| D. | 270<b<280 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com