
【题目】市场上经常见到的一种电池,总反应式为:Li+2Li0.35NiO2![]() 2Li0.85NiO2。负极材料是金属锂和碳的复合材料,含Li+导电固体为电解质,下列说法正确的是
2Li0.85NiO2。负极材料是金属锂和碳的复合材料,含Li+导电固体为电解质,下列说法正确的是
A.放电过程中Li+向正极移动
B.可加入硫酸以提高电解质的导电性
C.充电时,Li+向阳极移动
D.放电时,负极反应式为:2Li0.35NiO2+Li++e-═2Li0.85NiO2
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、Q是原子序教依次增大的五种短周期主族元素.其中只有Z是金属,W的单质是黄色固体, X、Y、W在周期表中的相对位里关系如图.下列说法正确的是
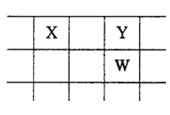
A. 五种元素中,原子半径最大的是W
B. Y的氢化物的沸点比W的氢化物的沸点低
C. Y与Z 形成的化合物都可以和盐酸反应
D. Z与Q形成的化合物的水解液一定显酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的甲烷在O2不足的情况下燃烧,得到CO、CO2和H2O的总质量为14.4 g,若其中水的质量为7.2 g,则CO的质量是( )
A.2.8g B.4.4g C.5.6g D.在2.8 g~5.6 g之间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯可通过石油裂解获得。下列有关乙烯的说法错误的是
A. 可以用作为水果的催熟剂
B. 不能使溴的CCl4溶液褪色
C. 能使酸性KMnO4溶液褪色
D. 在一定条件下,可自身加成形成聚乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应速率受很多因素影响.下列措施主要是从降低反应速率的角度考虑的是( )
A.将食物置于冰箱中冷藏保存
B.将FeCl3加入H2O2溶液中制备O2
C.将洗衣粉溶于温水后洗涤衣服
D.将CaCO3固体研磨后再与稀HCl反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定酸碱反应的中和热,计算时至少需要的数据是
①酸溶液的浓度和体积 ; ②碱溶液的浓度和体积 ;③比热容;④反应后溶液的质量;⑤ 生成水的物质的量;⑥反应前后温度的变化; ⑦操作所需的时间。
A.①②③⑥ B.③④⑤⑥ C.①③④⑤ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.恒温、恒压下,在一个可变容积的容器中发生如下反应:A(气)+B(气)![]() C(气)
C(气)
(1)若开始时放入1molA和1molB,到达平衡后,生成a molC,若开始时放入3mol A和3mol B,到达平衡后,生产C的物质的量为__________mol.
(2)若开始时放入x molA,2molB和1molC,到达平衡后,A和C的物质的量分别是ymol和3a mol,则x=__________mol,y=__________mol.平衡时,B的物质的量__________(选填一个编号)
(甲)大于2mol (乙)等于2mol (丙)小于2mol (丁)可能大于、等于或小于2mol
(3)若在(2)的平衡混合物中再加入3molC,待再次到达平衡后,C的物质的量分数是__________.
Ⅱ.若维持温度不变,在一个与(1)反应前起始体积相同、且容积固定的容器中发生上述反应。
(4)开始时放入1molA和1molB到达平衡后生成b molC.将b与(1)小题中的a进行比较a___________b(填<、>、=)。若保持温度、容积不变,改变某一条件使a=b,则反应物的转化率(填以下选项): (甲)增大 (乙)减小 (丙)不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中均需要的仪器是( )
①配制一定物质的量浓度的溶液 ②PH试纸的使用 ③过滤 ④蒸发
A. 试管 B. 胶头滴管
C. 玻璃棒 D. 漏斗
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com