
������Һ�и�����Ũ�ȹ�ϵ��ȷ����
| A��0.1 mol��L��1 NaHSO4��Һ�У�[Na��]��[SO42-]��[H��]��[OH��] |
| B��0.1 mol��L��1Na2S��Һ�У�2[Na��]��[S2��]��[HS��]��[H2S] |
| C��0.1 mol��L��1 NaHCO3��Һ�У�[Na��]��[H��]��[HCO3-]��2[CO32-]��[OH��] |
| D��������������ʵ���Ũ�ȵ�������Һ������������Һ��Ϻ�[Na��]��[CH3COO��]��[H��]��[OH��] |
C
�������������A��������������ˮ��ȫ�����H����Na����SO42-������0.1 mol��L��1 NaHSO4��Һ������Ũ�ȴ�С��ϵ��[H��]��[Na��]��[SO42-]��[OH��]��A����ȷ��B�����������غ��֪ 0.1 mol��L��1Na2S��Һ�У�[Na��]��2[S2��]��2[HS��]��2[H2S]��B����ȷ��C�����ݵ���غ��֪0.1 mol��L��1 NaHCO3��Һ�У�[Na��]��[H��]��[HCO3-]��2[CO32-]��[OH��]��C��ȷ��D�����������ᣬ�� ������������ʵ���Ũ�ȵ�������Һ������������Һ��Ϻ�ǡ�÷�Ӧ���ɵ�������ˮ�⣬��Һ�Լ��ԣ�����Һ������Ũ�ȴ�С��ϵ��[Na��]��[CH3COO��]��[OH��]��[H��]��D����ȷ����ѡC��
���㣺������Һ������Ũ�ȴ�С�Ƚϵ������ж�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����˵������ȷ����
| A����pH=4��ij��ϡ��10���������pH��5�������Ϊ���� |
B��0��1mol ��NaHCO3��Һ�� ��NaHCO3��Һ�� |
C��0��1mol ��NaHA��ҺPh=5������Һ�� ��NaHA��ҺPh=5������Һ��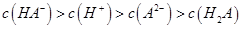 |
D��pH=4�Ĵ�����pH=10������������Һ�������ϣ�������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����������ȷ����
| A��NaHCO3��Һ�У�c(H+) + c(Na+)��c(HCO3��)+2c(CO32��) + c(OH��) |
| B��pH=12��Ba(OH)2��Һ��pH=12��Na2CO3��Һ�У�ˮ�����c(H��)һ���� |
| C��0.2mol��L��1 HCl��Һ������0.05 mol��L��1 Ba(OH)2��Һ��Ϻ���Һ��pH��1 |
| D����10 mL 0.10mol?L��1CH3COOH��Һ��������ʵ�����NaOH����Һ�����ӵ�Ũ���ɴ�С��˳���ǣ�c(Na+)��c(CH3COO��)��c(OH������c(H+) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����������25��ʱ��ˮ��Һ�еĵ���ƽ�ⳣ�����±�
| ���� | �����ᣨHCN�� | ̼�ᣨH2CO3�� | ����ᣨHF�� |
| ����ƽ�ⳣ��Kֵ | 6.2��10��10��K�� | 4.2��10��7��K1�� 5.6��10��11��K2�� | 6.61��10��4��K�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����й����⣬���ε�ˮ���йص���
�� NH4Cl��ZnCl2��Һ�������ӽ����еij����
�� ��NaHCO3��Al2(SO4)3������Һ������ĭ����
�� ��ľ�����̬���ʲ��ܻ��ʩ��
�� ʵ����ʢ��̼������Һ���Լ�ƿ������ĥ�ڲ�����
�� ��������AlCl3��Һ�õ�Al(OH)3����
| A���٢ڢ� | B���ڢۢ� | C���٢ܢ� | D���٢ڢۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
ij������Һ��ֻ��Na+��CH3COO-��H+��OH-�������ӡ�������������ȷ����
| A������Һ��pH��3��CH3COOH��pH��11��NaOH��Һ�������϶��� |
| B������Һ�ɵ����ʵ���Ũ�ȡ��������NaOH��Һ��CH3COOH��Һ��϶��� |
| C����������NaOH����Һ������Ũ��Ϊc(CH3COO-)��c(Na+)��c(OH-)��c(H+) |
| D������������ˮ��c(CH3COO-)һ������c(Na+)��c(NH4+)֮�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ʵ���Ũ����ͬ��������Һ�У�NH��+Ũ��������
| A��NH4Cl | B��NH4HCO3 | C��CH3COONH4 | D��NH4HSO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����½������ʵ�����NaCN��HCN����һ����ˮ�У��ټ�������ϡ���ᣬ������ҺpH=7������˵����ȷ���ǣ� ��
| A��δ����ϡ����֮ǰ��c(HCN)>c(Na+)>c( CN-) ��c(OH-)>c(H+) |
| B����ϡ�������Һ��c(CN-)+c��HCN��= c��Na+�� |
| C��pH=7ʱ����Һ�У�c( Na+)=" c(" CN-) |
| D����ϡ�����H2O�ĵ���̶ȼ�С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ж�����Һ�е�����������ȷ���ǣ� ��
| A����������м�ˮ����ɴ���ϡ��Һ�Ĺ���H+��Ũ����С |
| B����ϡ��Һ�У�H+��aq�� + OH-��aq�� �� H2O��l���� ��H����57.3kJ/mol����1 mol HClO��ϡ��Һ�ͺ�1 mol KOH��ϡ��Һ��ȫ��Ӧ�ų�����������57.3 kJ |
| C������ʱ��pH��2��CH3COOH��Һ��HCl��Һ��pH��12�İ�ˮ��NaOH��Һ��������Һ����ˮ�����c��H+����� |
| D�������£���ϡNaOH��Һ��CH3COOH��Һ��ϣ����ܳ���pH��7����c��OH-����c��Na+����c��H+����c��CH3COO-������� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com