
下列反应的离子方程式书写正确的是
A.铜溶于FeCl3溶液:3Cu+2Fe3+=3Cu2++2Fe
B.碳酸钙溶于醋酸:CO32-+2H+=CO2↑+H2O
C.AlCl3溶液中加入过量氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+
D.Ba(OH)2溶液中加入过量NaHCO3溶液:Ba2++HCO3-+OH-=BaCO3↓+H2O
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年甘肃省高一上第一次学段考试化学卷(解析版) 题型:选择题
下列对0.3 mol•L-1硫酸钾溶液的说法中,不正确的是 ( )
A.2L 溶液中含有0.6 mol SO42-离子
B.K+ 与SO42-离子的物质的量之比为2:1
C.1L 溶液中含溶质硫酸钾的物质的量为0.3 mol
D.2L 溶液中K+离子的物质的量浓度为1.2 mol•L-1
查看答案和解析>>
科目:高中化学 来源:2017届江苏省南通市如东县徐州市丰县高三10月联考化学卷(解析版) 题型:填空题
危化仓库中往往存有钠、钾、液氯、白磷(P4)、硝酸铵和氰化钠(NaCN)等危险品。请回答下列问题:
(1)钠、钾都为活泼金属,在空气中着火时会剧烈燃烧。若金属Na着火,应用 来扑(盖)灭。
(2)氯气是一种黄绿色的有毒气体,工业上常用NH3来检验氯气是否发生泄漏,检验时若产生白烟,证明氯气发生了泄漏,则白烟的主要成份是 。(填化学式)写出产生白烟化学方程式 。
(3)NH4NO3为爆炸物,在某温度下按下式进行分【解析】
5NH4NO3═4N2↑+2HNO3+9H2O,则被氧化和被还原的氮元素质量之比为 。
(4)硫酸铜溶液是白磷引起中毒的一种解毒剂:11P4+60CuSO4+96H2O═20Cu3P+24H3PO4+60H2SO4,若6molH3PO4生成,则被CuSO4氧化的P4的物质的量为 mol。
(5)NaCN属于剧毒物质,有一种处理方法其原理为:CN-与S2O32-反应生成两种离子,一种与Fe3+可生成红色溶液,另一种与H+作用产生能使品红溶液褪色的刺激性气体,写出离子反应方程式: 。
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三联合考试化学试卷(解析版) 题型:填空题
氨和联氨(N2H4)既是一种工业原料,又是一种重要的工业产品。
(1)实验室可用氯化铵与消石灰反应制取氨气,其反应的化学方程式为 。
(2)联氨在一定条件下可按下式分【解析】
3N2H4(g)=N2(g)+4NH3(g),已知断裂1molN—H、N—N及N≡N需吸收的能量依次为390.8kJ、193kJ、946kJ。若生成1molN2,则反应 (填“放出”或“吸收”) kJ的能量。
(3)NH3—O2燃料电池的结构如图所示。
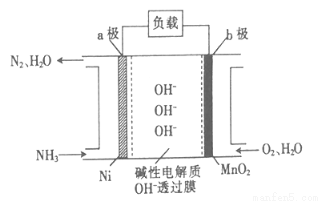
①a极为电池的 (填“正”或“负”)极。
②当生成1molN2时,电路中流过电子的物质的量为 。
(4)联氨可以高效地脱除烟道气中的NO从而生成N2,该反应中氧化产物与还原产物的物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三联合考试化学试卷(解析版) 题型:选择题
下列实验中,对应的现象以及结论都正确的是
选项 | 实验 | 现象 | 结论 |
A | 向酸性KMnO4溶液中滴加H2O2溶液至过量 | 紫色消失 | H2O2在该反应中作还原剂 |
B | 溶有SO2的BaCl2溶液中通入气体X | 有白色沉淀生成 | X一定是Cl2 |
C | 向FeBr2和KSCN混合溶液中滴入少量新制氯水,再加入CCl4混合振荡、静置 | 有机相呈红棕色,水相呈无色 | Fe2+的还原性大于Br- |
D | 铝丝用砂纸打磨后,放在冷的浓硝酸中浸泡一段时间后,放入CuSO4溶液中 | 铝丝表面变红色 | 铝可从铜盐溶液中置换出铜 |
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三联合考试化学试卷(解析版) 题型:选择题
2016年8月10日《生物谷》载文称,“毒性气体”CO、NO及H2S可作为新型药物开发的潜在靶点,用以开发更多新型药物来帮助治疗多种人类疾病。下列有关这三种气体的说法正确的是

A.都是电解质 B.都易溶于水
C.都能与碱溶液反应 D.都属于共价化合物
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上第一次联考化学试卷(解析版) 题型:选择题
下列各组离子能大量共存,当加入相应试剂后会发生化学变化,且发生反应的离子方程式正确的是()
选项 | 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
A | Fe2+、NO3-、NH4+ | NaHSO4溶液 | 3Fe2++NO3- +4H+=3 |
B | Ca2+、HCO3-、Cl- | 少量NaOH溶液 | Ca2++2HCO3- +2OH-=2H2O+CaCO3↓+CO32- |
C | K+、AlO2-、HCO3- --来源:Zxxk.Com] | 通入少量CO2 | 2Al |
D | NH4+、Al3+、SO42- | 少量Ba (OH) 2溶液 | 2NH4+ |
A.A B.B C. C D.D
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com