
【题目】有以下一系列反应,最终产物为乙二酸。

试回答下列问题:
(1)C的结构简式是______________。
B→C的反应类型是________________,
E→F的化学方程式是___________________。
(2)E与乙二酸发生酯化反应生成环状化合物的化学方程式是__________________。
(3)由B发生水解反应或C与H2O发生加成反应均生成化合物G。在乙二酸、水、苯酚、G四种分子中,羟基上氢原子的活泼性由强到弱的顺序是____________________。
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】实验室需要0.4 mol·L-1NaOH溶液450 mL
(1)配制上述溶液选用的主要玻璃仪器除烧杯、玻璃棒、胶头滴管外还需用到的玻璃仪器是____________(填仪器名称)。
(2)根据计算用托盘天平称取NaOH的质量为 _________g,在实验中其他操作均正确,若容量瓶用蒸馏水洗涤后没有干燥就开始移液,则所得溶液浓度 _____ 0.4 mol·L-1(填“大于”“等于”或“小于”,下同);若NaOH溶液在转移至容量瓶时未经冷却,则所得溶液浓度_____0.4mol·L-1;若定容时俯视液面,则所得溶液浓度_____0.4mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1.00L的容器中,通入一定量的N2O4 , 发生反应N2O4(g)2NO2(g),随温度的升高,混合气体的颜色变深.
回答下列问题:
(1)反应的△H0(填“大于”或“小于”);100℃时,体系中各物质浓度随时间变化如图所示.在0~60s时段,反应速率v(N2O4)为molL﹣1s﹣1;反应的平衡常数K1为 .
(2)100℃时达平衡后,改变反应温度为T,c(N2O4)以0.0020molL﹣1s﹣1的平均速率降低,经10s又达到平衡.
①T100℃(填“大于”或“小于”),判断理由是 .
②列式计算温度T时反应的平衡常数K2 .
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向(填“正反应”或“逆反应”)方向移动,判断理由是 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示某反应的能量变化,对于该图的理解,你认为一定正确的是( ) 
A.曲线Ⅰ和曲线Ⅱ分别表示两个化学反应的能量变化
B.曲线Ⅱ可表示反应2NH3 ![]() ?N2+3H2的能量变化
?N2+3H2的能量变化
C.该反应不需要加热就能发生
D.该反应的△H=E2﹣E1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组用如图1装置进行实验,试回答下列问题. 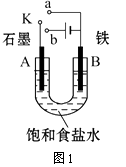
(1)若开始时开关K与a连接,则B极的电极反应式为 .
(2)若开始时开关K与b连接,则B极的电极反应式为 , 总反应的离子方程式为 . 有关上述实验,下列说法正确的是(填序号) .
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24L气体,则溶液中转移0.2mol电子
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图2装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾. 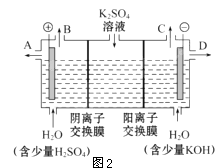
①该电解槽的阳极反应式为 .
此时通过阴离子交换膜的离子数(填“大于”、“小于”或“等于”)通过阳离子交换膜的离子数.
②若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于一些有机物在合适条件下的化学反应说法正确的是( )
A.![]() 能催化氧化生成醛
能催化氧化生成醛
B. 能在浓硫酸的作用下生成烯
能在浓硫酸的作用下生成烯
C.CH3Br 能在氢氧化钠的乙醇溶液的作用下生成醇
D.![]() 既能与酸反应也能与碱反应生成盐
既能与酸反应也能与碱反应生成盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
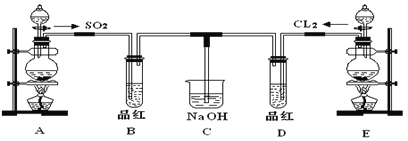
(1)实验室用装置A制备SO2。某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是:________________________________________________________
(2)实验室用装置E制备CL2,其反应的化学化学方程式为:MnO2+4HCl(浓)==MnCl2+Cl2 ↑ +2H2O请指出该反应中的液体反应物在反应中所表现出的化学性质:_______________________________________。
(3)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:B:________________________________,D:____________________________。
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B:________________________________,D:____________________________。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强,他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F(C21H20O6)在临床医学上具有预防肿瘤的作用,其合成路线如下:其中反应③中反应物的原子利用率为100%.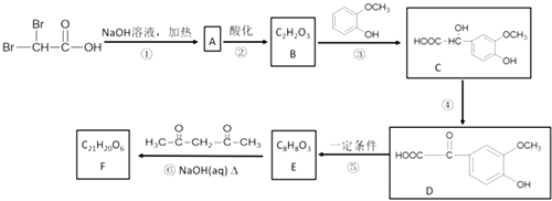
已知:
(a) 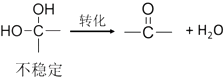
(b) ![]()
(c) ![]()
请回答下列问题:
(1)B中含有的官能团名称是 . ③的反应类型为
(2)反应①的化学方程式是 . 反应④的化学方程式是 .
(3)E的结构简式是 . F的结构简式是 .
(4)E的同分异构体中,同时符合下列两个条件的共有种,其中核磁共振氢谱中有4组吸收峰的同分异构体的结构简式为
①苯环上的一取代物只有2种;
②1mol该物质与足量NaOH溶液反应时,反应消耗3mol NaOH.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com