
【题目】已知NA是阿伏加德罗常数的值,下列说法错误的是
A.48 g正丁烷和10 g异丁烷的混合物中共价键数目为13NA
B.1.0 mol CH4与Cl2在光照下反应生成的CH3Cl分子数为1.0NA
C.标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA
D.4.5 g SiO2晶体中含有的硅氧键数为0.3NA
【答案】B
【解析】
A.正丁烷和异丁烷只是碳架不同,分子中含有的共价键数均为13条,所以48g正丁烷和10g异丁烷,即混合物的物质的量为n=![]() ,所以48g正丁烷和10g异丁烷的混合物中共价键数目为13NA,故A正确;
,所以48g正丁烷和10g异丁烷的混合物中共价键数目为13NA,故A正确;
B.CH4与Cl2的在光照下发生的取代反应产物是多种氯代烃的混合物,不是完全生成CH3Cl,所以1.0 mol CH4与Cl2在光照下反应生成的CH3Cl分子数小于1.0NA,故B错误;
C.标况下11.2L混合气体的物质的量n=![]() =0.5mol,而甲烷和乙烯中均含4个H原子,故0.5mol混合物中H原子数为2NA个,故C正确;
=0.5mol,而甲烷和乙烯中均含4个H原子,故0.5mol混合物中H原子数为2NA个,故C正确;
D.4.5gSiO2晶体的物质的量为:![]() ,每摩尔二氧化硅含有4mol硅氧键,所以4.5gSiO2晶体含有硅氧键数目为:0.075mol×4×NAmol1=0.3NA,故D正确;
,每摩尔二氧化硅含有4mol硅氧键,所以4.5gSiO2晶体含有硅氧键数目为:0.075mol×4×NAmol1=0.3NA,故D正确;
答案选B。


科目:高中化学 来源: 题型:
【题目】(1)基态Fe原子的简化电子排布式为______________________。
(2)常温下,Fe(CO)5为黄色液体,易溶于非极性溶剂。写出CO的电子式______________;Fe(CO)5分子中σ键与π键之比为______________。
(3)Ni能与类卤素(SCN)2反应生成Ni(SCN)2。Ni(SCN)2中第一电离能最大的元素是_____________;(SCN)2分子中硫原子的杂化方式是_____________;
(4)硝酸铜溶于氨水形成[Cu(NH3)4](NO3)2的深蓝色溶液。
①[Cu(NH3)4](NO3)2中阴离子的立体构型是_________________。
②与NH3互为等电子体的一种阴离子为_____________(填化学式);氨气在一定的压强下,测得的密度比该压强下理论密度略大,请解释原因__________。
(5)金属晶体可看成金属原子在三维空间中堆积而成,单质铝中铝原子采用铜型模式堆积,原子空间利用率为74%,则铝原子的配位数为________________。
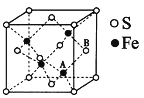
(6)铁和硫形成的某种晶胞结构如右图所示,晶胞参数a=xpm,则该物质的化学式为___________________;A原子距离B原子所在立方体侧面的最短距离为________________pm(用x表示); 该晶胞的密度为____________g·cm-3。(阿伏加德罗常数用NA表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在利用镁条与醋酸的反应研究化学反应速率的影响因素的实验中,同学们记录了相同体积、不同浓度的醋酸与足量Mg条反应,产生H2体积随时间变化的数据,并以单位时间内产生H2的体积来表示反应速率,其反应速率随时间变化的图(如图所示)。
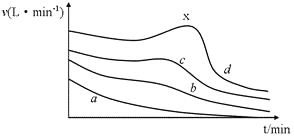
(1)在a、b、c、d四条曲线中,对应醋酸溶液的物质的量浓度最小的是_________,反应最后产生的H2在相同条件下体积最大的是_____________。
(2)在d曲线中,反应一段时间以后,反应速率出现反常的升高的现象(x点附近)。产生这种现象的原因主要是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】抗结肠炎药物Y结构如图所示,以下说法错误的是

A. 该有机物既能和酸反应又能和碱反应
B. 1mol该有机物可以和2molNaOH发生反应
C. 该有机物可以发生缩聚反应
D. 该有机物不能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三盐基硫酸铅(3PbO·PbSO4·H2O)简称“三盐”,白色或微黄色粉末,热稳定性能优良,主要用作聚氯乙烯的热稳定剂。“三盐”是由可溶性铅盐中加入硫酸生成硫酸铅,再加氢氧化钠而制得。以100.0吨铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如下图所示

已知:(1)Ksp(PbSO4)=1.82×10-8,Ksp(PbCO3)=1.46×10-13;
(2)铅与冷盐酸、冷硫酸几乎不起作用。
请回答下列问题:
(1)写出步骤①“转化”的化学方程式_________________________________
(2)步骤②“过滤1”后所得滤渣的主要成分为_____________
(3)步骤③“酸溶”,最适合选用的酸为___________,为提高酸溶速率,可采取的措施是____________________________________(任意写出一条)
(4)若步骤④“沉铅”后的滤液中c(Pb2+)=1.82×10-5mol·L-1,则此时c(SO42-)=_________ mol·L-1
(5)从原子利用率的角度分析该流程的优点为____________________________________。
(6)步骤⑥“合成”三盐的化学方程式为____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃是一类简单的有机化合物。
(1)天然气属于______________(填“纯净物”或“混合物”),其组成以__________为主。该分子的电子式是_____________,其空间结构是_____________________。
(2)烷烃随着碳原子数的增多,沸点逐渐________(填“升高”或“降低”),碳原子数≤________的烷烃呈气态,它们和氯气发生取代反应的条件是________________。
(3)2,2,3-三甲基丁烷的结构简式是____________________________________,其一氯代物有_______种,该烷烃与正庚烷互为__________________________(填“同系物”或“同分异构体”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油是工业的血液,与我们的生产、生活息息相关。
某烃A是重要的石油化工产品。其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应。回答下列问题。
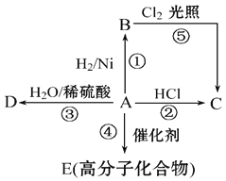
(1)物质A的工业制法是_____________________________。
(2)与A互为同系物的是______________________。(选填编号)
a CH3CH=CH2 b CH2=CHCH=CH2 c CH≡CH d CH3CH3
(3)高分子化合物E可用于制食品包装袋,写出其结构简式为_____________________;D是酒的主要成分,写出其结构简式为___________________________________。
(4)写出②⑤两步反应的化学方程式,并注明反应类型(有机物写结构简式)。
②__________________________________________反应类型________________
⑤__________________________________________反应类型________________
(5)苯是一种特殊的不饱和烃。若要鉴别苯与烯烃,可选用的试剂是______________。
(6)聚氯乙烯,简称PVC是一种在建筑材料、工业制品等方面广泛应用的通用塑料,若以乙炔为原料合成聚氯乙烯,请在方框内填写相应的物质,有机物写结构简式。
CH≡CH PVC
PVC
_____________________、_______________________
(7)异戊二烯是重要的有机化工原料,其结构简式为CH2=C(CH3)CH=CH2,它与溴水反应最多可以得到_________种产物。若烃X与异戊二烯具有相同的分子式,与Br2/CCl4反应后得到3-甲基-1,1,2,2-四溴丁烷,则烃X的结构简式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】瑞德西韦(Remdesivir)是一种核苷类似物,具有抗病毒活性,对新型冠状病毒(2019-nCoV)病例展现出较好的疗效。其结构如图a所示,回到下列问题:
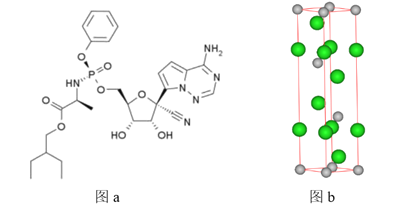
(1)该结构中P原子价电子的轨道表示式为_________。
(2)该结构中处于第二周期原子第一电离能从大到小的顺序为_______(用化学用语回答)。
(3)该结构氨基中N的杂化方式为_________,该分子间的作用力有________。
(4)苯酚(C6H5OH)为合成反应物之一,苯酚的晶体类型是_________,与甲苯(![]() )的相对分子质量相近,但苯酚的熔沸点高于甲苯,原因是________。
)的相对分子质量相近,但苯酚的熔沸点高于甲苯,原因是________。
(5)某镨(59Pr)的化合物是合成该分子的催化剂之一,则镨元素位于元素周期表中的__________区。MgCl2也是合成瑞德西韦的催化剂,晶胞如图b所示,则Mg2+处于氯离子围成的___________空隙中。晶胞参数为acm、acm、bcm,则该晶体的密度为_____________g/cm3。(填表达式,已知底面夹角分别为120°、60°,侧面与底面垂直)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见的五种盐X、Y、Z、M、N,它们的阴离子可能是SO42-、Cl-、NO3-、CO32-,阳离子可能是Ag+、NH4+、Na+、Al3+、Cu2+、Ba2+、Fe3+,已知:①M的焰色反应呈黄色。②五种盐均能溶于水,水溶液均为无色。③X的溶液呈中性,Y、Z、N的溶液呈酸性,M的溶液呈碱性。④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有X、Z的溶液不产生沉淀。⑤若在这五种盐的溶液中,分别加入氨水,N和Z的溶液中生成沉淀,继续加氨水,Z中沉淀消失。⑥把X的溶液分别加入到Y、Z、N的溶液中,均能生成不溶于稀硝酸的沉淀。请回答下列问题:
(1)五种盐中,所含阴离子相同的两种盐的化学式是______________。
(2)M溶液显碱性的原因是(用离子方程式表示)_______________________。
(3)X和Z的溶液反应的离子方程式是______________________________。
(4)N和氨水反应的离子方程式是_____________________________________。
(5)若要检验Y中所含的阳离子,正确的实验方法是_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com