


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.10mol/L醋酸溶液中粒子浓度的关系满足:c(CH3COOH)>c(H+)>c(CH3COO-)>c(OH-) |
| B.0.10mol/L的CH3COOH溶液中加水稀释,溶液中c(OH-)减小 |
| C.CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动 |
| D.常温下pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液pH<7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
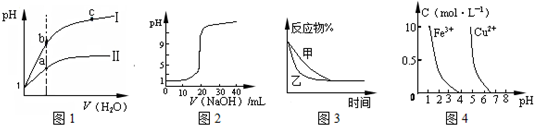
| A.图1表示同温度下,pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强 |
| B.图2表示0.1000mol?L-1CH3COOH溶液滴定20.00mL0.1000mol?L-1NaOH溶液所得到的滴定曲线 |
| C.图3表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强比甲的压强大 |
| D.据图4,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在4左右 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.向冰醋酸中加水至配成醋酸稀溶液的过程中H+的浓度逐渐减小 |
| B.对于物质的量浓度相同的氢氧化钠和氨水,加水稀释至m倍、n倍后,若稀释后溶液的PH相等,则m<n |
| C.常温下,5ml0.02mol/LHCl溶液与5ml0.02mol/LBa(OH)2溶液混合,经充分反应后,如果溶液体积为10mL,则溶液的pH=12 |
| D.常温下将稀NaOH溶液与醋酸溶液混合,可能出现PH>7的情况,且c(OH-)>c(Na+)>c(CH3COO-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.3.0-3.3 | B.3.3-3.5 | C.3.5-4.0 | D.3.7-4.3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| H2CO3 | Ka1=4.3×10-7 | H2C2O4 | Ka1=5.6×10-2 |
| Ka2=5.6×10-11 | Ka2=5.42×10-5 |
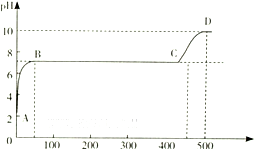
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.NaCl的电子式为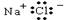 |
| B.NaCl的水溶液是强电解质 |
| C.23Na37Cl中质子数和中子数之比是8:7 |
| D.电解熔融氯化钠可得到氯气和金属钠 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com