
【题目】乙醇是一种重要的化工原料,由乙醇为原料衍生出的部分化工产品如图所示:
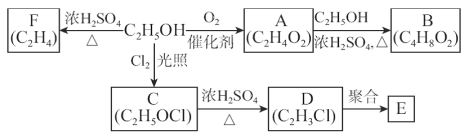
回答下列问题:
(1)D中的官能团名称是________________。
(2)E是一种常见的塑料,其化学名称是___________。
(3)由乙醇生成C的反应类型为___________________。
(4)A→B反应的化学方程式为___________________________。
(5)实验室制取F的化学方程式为_____________。
(6)检验C中非含氧官能团的试剂及方法是____________________。
【答案】氯原子、碳碳双键 聚氯乙烯 取代反应 CH3COOH + CH3CH2OH![]() CH3COOC2H5+H2O CH3CH2OH
CH3COOC2H5+H2O CH3CH2OH ![]() CH2=CH2↑+H2O 将C在氢氧化钠的水溶液中加热水解,然后先加入稀硝酸酸化,再加入硝酸银溶液,若出现白色沉淀,则证明有氯原子
CH2=CH2↑+H2O 将C在氢氧化钠的水溶液中加热水解,然后先加入稀硝酸酸化,再加入硝酸银溶液,若出现白色沉淀,则证明有氯原子
【解析】
乙醇在浓硫酸加热条件下得到F,F为乙烯,催化氧化得到A,A为乙酸,A可以和乙醇发生反应生成B,B为乙酸乙酯,E由氯乙烯聚合得到,E为聚氯乙烯。
(1)D是氯乙烯,D中的官能团名称是碳碳双键和氯原子;
(2)E是一种常见的塑料,由氯乙烯聚合得到,是聚氯乙烯;
(3)由乙醇生成C的反应类型为取代反应;
(4)A→B为酯化反应,反应的化学方程式为CH3COOH + CH3CH2OH![]() CH3COOC2H5+H2O;
CH3COOC2H5+H2O;
(5)实验室采取乙醇分子内脱水制取F,化学方程式为CH3CH2OH ![]() CH2=CH2↑+H2O;
CH2=CH2↑+H2O;
(6)C中非含氧官能团为氯离子,通常采取将其变为溶液中的氯离子的形式进行检验,检验方法为将C在氢氧化钠的水溶液中加热水解,然后先加入稀硝酸酸化,再加入硝酸银溶液,若出现白色沉淀,则证明有氯原子。


科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A.向沸水中滴加FeCl3溶液制备胶体: Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
B.在H2SO4溶液中滴入Ba(OH)2溶液至溶液呈中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O
C.钠与CuSO4溶液反应:2Na+Cu2+=Cu +2Na+
D.Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:还原性强弱:I->Fe2+。往100 mL碘化亚铁溶液中缓慢通入3.36 L(标准状况)氯气,反应完成后溶液中有一半的Fe2+被氧化成Fe3+。则原碘化亚铁溶液的物质的量浓度为
A. 1.2 mol·L-1 B. 1.5 mol·L-1 C. 1.0 mol·L-1 D. 1.1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通常利用SiO2 和碳反应来制取硅,写出反应的化学方程式___________________。
工业上还可以利用镁制取硅,反应为2Mg+SiO2 = 2MgO+Si,同时会发生副反应:2Mg + Si = Mg2Si。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:

(1)由于O2和H2O(g)的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用________(填序号)。
a.石灰石 b.锌粒 c.纯碱
(2)实验开始时,必须先通一段时间X气体,再加热反应物,其理由是 ___________________________;当反应引发后,移走酒精灯,反应能继续进行,其原因是______________________。
(3)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸,可观察到闪亮的火星,产生此现象的原因是副产物Mg2Si遇盐酸迅速反应生成SiH4(硅烷)气体,然后SiH4自燃.用化学方程式表示这两个反应①________________________②___________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将20 g NaOH固体溶于水配成100 mL溶液,其密度为1.185 g·mL-1。
(1)该溶液中NaOH的物质的量浓度为______mol·L-1。
(2)从该溶液中取出10 mL,其中NaOH的物质的量浓度为_____ mol· L-1,含NaOH的物质的量为______mol。
(3)将取出的10 mL溶液加水稀释,稀释后溶液中NaOH的物质的量浓度为1 mol·L-1,稀释后溶液体积为___ mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知一定温度和压强下,合成氨反应:N2(g)+3H2(g)=2NH3(g) ΔH=-92.0 kJ/mol,将1 mol N2和3 mol H2充入一密闭容器中,保持恒温恒压,在催化剂存在时进行反应,达到平衡时,测得N2的转化率为20%。若在相同条件下,起始时向该容器中充入2 mol NH3,反应达到平衡时的热量变化是( )
A.吸收18.4 kJ热量B.吸收73.6 kJ热量
C.放出18.4 kJ热量D.放出73.6 kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】容积均为1L的甲、乙两个恒容容器中,分别充入2molA、2molB和1molA、1molB,相同条件下,发生下列反应:A(g)+B(g)![]() xC(g) △H<0。测得两容器中c(A)随时间t的变化如图所示,下列说法不正确的是
xC(g) △H<0。测得两容器中c(A)随时间t的变化如图所示,下列说法不正确的是
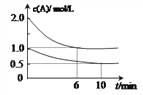
A. x=1
B. 此条件下,该反应的平衡常数K=4
C. 给乙容器升温可缩短反应达平衡的时间但不能提高平衡转化率
D. 甲和乙中B的平衡转化率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学为了获取在Fe(OH)2制备过程中,沉淀颜色的改变与氧气有关的实验证据,用下图所示装置进行了如下实验(夹持装置已略去,气密性已检验)。
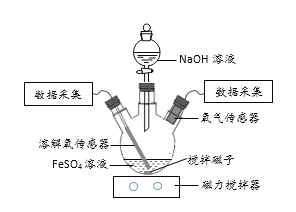
(进行实验)
实验步骤:Ⅰ.向瓶中加入饱和FeSO4溶液,按图1所示连接装置;
Ⅱ.打开磁力搅拌器,立即加入10% NaOH溶液;
Ⅲ.采集瓶内空气中O2含量和溶液中O2含量(DO)的数据。
实验现象:生成白色絮状沉淀,白色沉淀迅速变为灰绿色,一段时间后部分变为红褐色。
实验数据:
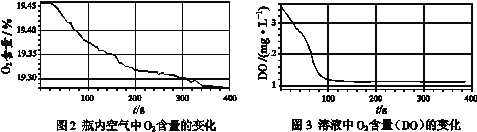
(解释与结论)
(1)搅拌的目的是__________________________。
(2)生成白色沉淀的离子方程式是____________。
(3)红褐色沉淀是__________________________。(填化学式)
(4)通过上述实验,可得到“在Fe(OH)2制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是______________________。
(5)写出白色沉淀最终生成红褐色转化的方程式:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持、加热和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是
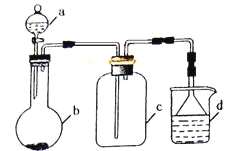
选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓硝酸 | Cu | NO2 | NaOH溶液 |
B | 浓氨水 | CaO | NH3 | H2O |
C | 稀硝酸 | Cu | NO | H2O |
D | 浓硫酸 | Cu | SO2 | 饱和NaHSO3溶液 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com