
【题目】现有A、B、C、D四种短周期主族元素,它们的原子序数依次增大,其中A元素原子核外电子仅有一种原子轨道,也是宇宙中最丰富的元素,B元素原子的核外p轨道电子数比s轨道电子数少1,C为金属元素且原子核外p轨道电子数和s轨道电子数相等,D元素的原子核外所有p轨道全充满或半充满。
(1)写出四种元素的元素符号:A_______,B_______,C_______,D_______。
(2)写出C、D两种基态原子核外电子排布图:
C__________________________________;
D___________________________________。
(3)写出B、C两种元素的单质在一定条件下反应的化学方程式:_________。
(4)写出B元素单质和简单氢化物的电子式:单质____________,氢化物____________。
【答案】H N Mg P ![]()
![]() 3Mg+N2
3Mg+N2![]() Mg3N2
Mg3N2 ![]()
![]()
【解析】
有A、B、C、D四种短周期主族元素,它们的原子序数依次增大,其中A元素原子核外电子仅占据一种原子轨道,也是宇宙中最丰富的元素,则A为氢元素;B元素原子的核外p轨道电子数比s轨道电子数少1, B原子核外电子排布为1s22s22p3,为氮元素;C为金属元素且原子核外p轨道电子数和s轨道电子数相等,处于第三周期,核外电子排布为1s22s22p63s2,则C为镁元素,D元素的原子核外所有p轨道全充满或半充满,原子序数大于Mg,则核外电子排布为1s22s22p63s23p3,则D为磷元素,据此分析。
有A、B、C、D四种短周期主族元素,它们的原子序数依次增大,其中A元素原子核外电子仅占据一种原子轨道,也是宇宙中最丰富的元素,则A为氢元素;B元素原子的核外p轨道电子数比s轨道电子数少1,B原子核外电子排布为1s22s22p3,为氮元素;C为金属元素且原子核外p轨道电子数和s轨道电子数相等,处于第三周期,核外电子排布为1s22s22p63s2,则C为镁元素;D元素的原子核外所有p轨道全充满或半充满,原子序数大于Mg,则核外电子排布为1s22s22p63s23p3,则D为磷元素。
(1)由上述分析可知,A为H;B为N;C为Mg;D为P;
(2)C为Mg,D为P,基态原子核外电子排布图分别为![]() 、
、![]() ;
;
(3)镁在氮气中燃烧生成氮化镁,反应方程式为3Mg+N2![]() Mg3N2;
Mg3N2;
(4)氮气和氨气的电子式分别为![]() 、
、![]() 。
。


 名师点拨卷系列答案
名师点拨卷系列答案科目:高中化学 来源: 题型:
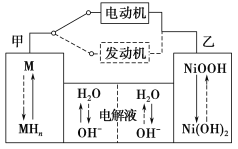
【题目】第三代混合动力车,可以用电动机、内燃机或二者结合推动车辆汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在刹车或下坡时,电池处于充电状态。
(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,生成1 mol水蒸气放热569.1 kJ。则该反应的热化学方程式为_____________。
(2)混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解质溶液。镍氢电池充放电原理示意如图,其总反应式为H2+2NiOOH ![]() 2Ni(OH)2。根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH_____(填“增大”、“减小”或“不变”),该电极的电极反应式为___________。
2Ni(OH)2。根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH_____(填“增大”、“减小”或“不变”),该电极的电极反应式为___________。
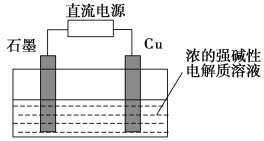
(3)Cu2O是一种半导体材料,可通过如图所示的电解装置制取,电解总反应式为2Cu+H2O![]() Cu2O+H2↑,阴极的电极反应式是____________________。用镍氢电池作为电源进行电解,当电池中有1 mol H2被消耗时,Cu2O的理论产量为________g。
Cu2O+H2↑,阴极的电极反应式是____________________。用镍氢电池作为电源进行电解,当电池中有1 mol H2被消耗时,Cu2O的理论产量为________g。
(4)远洋轮船的钢铁船体在海水中易发生电化学腐蚀。为防止这种腐蚀,通常把船体与浸在海水里的Zn块相连,或与像铅酸蓄电池这样的直流电源的________(填“正”或“负”)极相连。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W为原子序数递增的四种短周期元素,其中Y、Z为金属元素。X、Y、Z、W的最高价氧化物对应的水化物甲、乙、丙、丁之间存在如图所示反应关系(关系图中“—”相连的两种物质能发生反应)。下列判断正确的是

A. X是元素周期表中非金属性最强的元素 B. Z位于元素周期表第3周期IA族
C. 四种原子中,Y原子半径最小 D. W的简单阴离子可能促进水的电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银铜合金广泛用于航空工业,从银铜合金的切割废料中回收银并制备透明半导电薄膜材料(CuAlO2)的工艺如下:
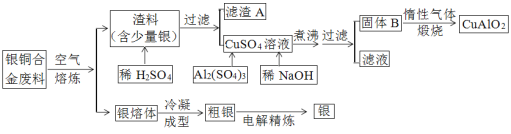
注:Al(OH)3和Cu(OH)2分解的温度分别为450℃和80℃。
(1)加快渣料(含少量银)溶于稀H2SO4的速率的措施有_______(写出一种)。
(2)滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,写出滤渣A中银与稀HNO3反应的化学方程式为_______。
(3)煮沸CuSO4混合溶液的过程中,得到固体B,则固体B的成分为_______;在生成固体B的过程中,需控制NaOH的加入量和防止滴加时NaOH的量局部过大,可防止加入NaOH的量局部过大的操作是_______。若NaOH过量,则因过量引起的反应的离子方程式为_______。
(4)已知:在常温下Cu(OH)2的Ksp=2×1020 mol3·L3,则常温下0.02 mol·L1CuSO4溶液里,如要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于_________。
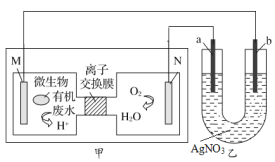
(5)图中甲为微生物将有机废水的化学能转化为电能的一种新型污水处理装置,利用该装置进行电解精炼银时,粗银应为乙装置的_______(填“a”或“b”)极,b电极反应式为_______。当N电极消耗1.12 L(标准状况下)O2时,则乙装置中理论上能产生_______ g银。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,取浓度均为0.1 mol·L1的醋酸溶液和氨水各20 mL,分别用0.1 mol·L1 氢氧化钠溶液和0.1 mol·L1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示。下列说法正确的是
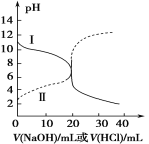
A.曲线I,滴加10 mL溶液时:c(NH4+)+c(H+)=c(OH-)+c(NH3·H2O)
B.曲线I,滴加20 mL溶液时:两溶液恰好完全反应,此时溶液的pH<7
C.曲线II,滴加溶液体积在10~20 mL之间时存在:c(NH4+)=c(Cl-)>c(OH-)=c(H+)
D.曲线II,滴加30 mL溶液时:c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低、燃料易于贮运及污染小等特点。如图所示为镁-次氯酸盐燃料电池的工作原理图,下列有关说法不正确的是( )
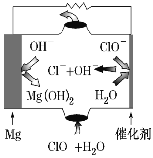
A.该燃料电池中镁为负极,发生氧化反应
B.正极反应为ClO-+H2O+2e-===Cl-+2OH-
C.电池总反应为Mg+ClO-+H2O===Mg(OH)2+Cl-
D.放电过程中OH-移向正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设水的电离平衡线如右图所示。

(1)若以A点表示25℃时水在电离平衡时的粒子浓度,当温度升高到100℃时,水的电离平衡状态到B点,则此时水的离子积从___________增加到____________;
(2)将PH=8的Ba(OH)2溶液与PH=5的稀盐酸混合,并保持在100℃的恒温,欲使混合溶液的PH=7,则Ba(OH)2溶液和盐酸的体积比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,装置正确且能达到实验目的的是
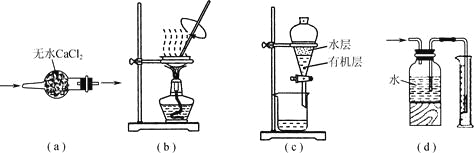
A.用图a所示装置干燥SO2气体
B.用图b所示装置蒸发CH3COONa溶液得醋酸钠晶体
C.用图c所示装置分离有机层与水层,水层从分液漏斗下口放出
D.用图d所示装置测量氯气的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,对应的现象以及结论都正确且两者具有因果关系的是![]()
选项 | 实验 | 现象 | 结论 |
A | 向2mL | 黄色逐渐消失,加KSCN溶液颜色不变 | 还原性: |
B | 往 | 产生白色胶状沉淀 | 酸性: |
C | 常温下将铝片加入浓硝酸中 | 无明显现象 | 铝与浓硝酸不反应 |
D | 将 | 紫色溶液褪色 |
|
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com