
【题目】下列变化中,加入氧化剂才可以实现的是( )
A. Cl2→Cl- B. H+ → H2 C. Na2O → NaOH D. Cu → Cu2+
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:
【题目】下列鉴别Na2CO3和NaHCO3两种白色粉末的方案不能达到预期目的的是
A. 分别向等物质的量的白色粉末中加入足量盐酸,充分反应后,比较产生气体的体积
B. 分别向等物质的量的白色粉末中加入等体积、等浓度的稀盐酸,比较生成气体的快慢
C. 分别用图示装置进行实验,观察澄清石灰水是否变浑浊

D. 分别配成相同浓度溶液,滴加2滴酚酞试液后,比较溶液颜色的深浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列九种物质:①H2O,②Al,③CO2,④盐酸,⑤硫酸钡,⑥NaOH⑦饱和FeCl3溶液,⑧氨水,⑨乙醇。根据上述提供的物质,回答下列问题:
(1)属于电解质的是 _______________________(填序号),属于非电解质__________(填序号)。
(2)上述物质间发生的某反应的离子方程式为H++OH===H2O,则该反应的化学方程式为_________________________________________________________________________。
(3)实验室制备少量Fe(OH)3胶体所用的物质有__________(填序号),反应的离子方程式为____________________________________________________________________________。
(4)Al和Na的单质同时加入到一定量的水中,充分反应后,发现既无沉淀生成又无固体残留物存在,请用两个离子方程式表示其变化:______________________________; ____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示。

(1)只根据图I、II所示实验,能够达到实验目的是(填装置序号)__________________;
(2)图III、IV所示实验均能鉴别这两种物质,与实验III相比,实验IV的优点是_________;(填选项序号)
A.IV比III复杂 B.IV比III安全
C.IV比III操作简便 D.IV可以做到用一套装置同时进行两个对比实验,而III不行
(3)若用实验IV验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是___________________;
(4)将碳酸氢钠溶液与澄清石灰水混合并充分反应。当碳酸氢钠溶液过量时,其离子方程式为__________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物含有C、H、O三种元素,其质谱如图所示.将4.3g该有机物在O2中充分燃烧,使生成物依次通过足量浓硫酸和碱石灰,浓硫酸增重2.7g,碱石灰增重8.8g,则: 
(1)该有机物的摩尔质量为 .
(2)该有机物的分子式为 .
(3)1mol该有机物与足量的金属钠反应产生1mol氢气,核磁共振氢谱有两个峰,且面积比为2:1,请写出其结构简式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同类物质性质相似,SO2和CO2同属于酸性氧化物,性质类似。下列说法不正确的是( )
A. SO2与澄清石灰水反应生成白色沉淀CaSO3 B. SO2与BaO反应,生成BaSO3
C. SO2与水反应生成H2SO3 D. SO2和Na2O反应生成Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
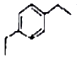
【题目】已知烯烃与苯在一定条件下反应生成芳香烃,如: ![]() +H2C=CH2
+H2C=CH2 ![]()
![]()
![]() +2H2C=CH2
+2H2C=CH2 ![]()
![]() +2H2C=CH2
+2H2C=CH2 ![]()
![]()
丙烯是三大合成材料的基本原料,可用于合成应用广泛的DAP树脂单体和双酚等有机物,具有重要的工业用途.
(1)写出丙烯在一定条件下发生聚合反应的化学方程式 .
(2)丙烯与苯在一定条件下反应可生成M、N等多种芳香烃.红外光谱、核磁共振是研究机物结构的重要方法,根据下列数据,写出M,N的结构简式. M:元素组成:C89.99%、H 10.06%;1H核磁共振有5个信号.
N:元素组成:C88.82%、H11.18%;1H核磁共振有3个信号.
M: , N: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为测定Na2CO3固体(含少量NaCl)的纯度,设计如图装置(含试剂)进行实验. 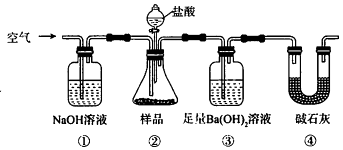
下列说法不正确的是( )
A.必须在②③间添加吸收HCl的装置
B.④的作用是防止空气中的气体影响实验的精确度
C.通入空气的作用是保证②中产生的气体完全转移到③中
D.称取样品和③中产生的沉淀的质量即可求算Na2CO3固体的纯度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】弱电解质的电离平衡、盐类的水解平衡和难溶物的溶液平衡均属于化学平衡. I、已知H2A在水中存在以下平衡:H2AH++HA﹣ , HA﹣H++A2﹣ .
(1)NaHA溶液的pH(填大于、小于或等于) Na2A溶液的pH.
(2)某温度下,若向0.1mol/L的NaHA溶液中逐滴滴加0.1mol/L KOH溶液至溶液呈中性.此时该混合溶液中下列关系中,一定正确的是 . a.c(H+)c(OH﹣)=1×10﹣14 b.c(Na+)+c(K+)=c(HA﹣)+2c(A2﹣)
c.c(Na+)>c(K+) d.c(Na+)+c(K+)=0.05mol/L
(3)已知常温下H2A的钙盐(CaA)饱和溶液中存在以下平衡:CaA(s)Ca2+(aq)+A2﹣(aq)△H>0. ①降低温度时,Ksp(填“增大”、“减小”或“不变”).
②滴加少量浓盐酸,c(Ca2+)(填“增大”、“减小”或“不变”).
(4)II、含有Cr2O72﹣的废水毒性较大,某工厂废水中含5.00×10﹣3 molL﹣1的Cr2O72﹣ . 为使废水能达标排放,作如下处理: Cr2O72﹣ ![]() Cr3+、Fe3+
Cr3+、Fe3+ ![]() Cr(OH)3、Fe(OH)3
Cr(OH)3、Fe(OH)3
①该废水中加入绿矾(FeSO47H2O)和H+ , 发生反应的离子方程式为: .
②欲使10L该废水中的Cr2O72﹣完全转化为Cr3+ , 理论上需要加入g FeSO47H2O.
③若处理后的废水中残留的c(Fe3+)=2×10﹣13molL﹣1 , 则残留的Cr3+的浓度为 . (已知:Ksp[Fe(OH)3]=4.0×10﹣38 Ksp[Cr(OH)3]=6.0×10﹣31)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com