
����Ŀ������240mL 0.4molL��1��Na2CO3��Һ���Իش��������⣺
��1��ѡ����������ɱ�ʵ��������������У�������ƽ����ȷ��0.1g����ҩ�ס��ձ����������� �� �ȣ�
��2�����㣺��ҪNa2CO3���������Ϊ ��
��3������������������Na2CO3����Ӧ����С�ձ��в�������ƽ�� ��������������������������
��4��ת�ơ�ϴ�ӣ���ת��ʱӦʹ�� ������ϴ���ձ�2��3����Ϊ�� ��
��5�����ݡ�ҡ�ȣ����ݵIJ����� ��
��6��ijѧ��ʵ������Na2CO3��Һ��Ũ��Ϊ0.39molL��1��ԭ������� ������ĸ����
A��ʹ����ֽ����Na2CO3����
B������ƿ��ԭ��������������ˮ
C���ܽ����ձ�δ�����ϴ�ӣ�
���𰸡���1��250mL����ƿ����ͷ�ιܣ�
��2��10.6g��
��3�����̣�
��4������������֤����ȫ��ת��������ƿ�У�
��5��������ƿ�м�������ˮ����̶���1 cm��2 cmʱ�����ý�ͷ�ιܵμ�����ˮ��Һ��İ�Һ����ʹ��Ϳ̶������У�
��6��C��
�������������������1����������һ�����ʵ���Ũ�ȵ���Һ����ѡ��������Ȼ���жϻ�ȱ�ٵ�������
��2������m=cVM�������ʵ�������
��3������ʱ�������룻
��4����ҺʱΪ��ֹҺ��������Ӧ�ò�����������ϴ���ձ�2�Ρ�3����Ϊ�˱�֤����ȫ��ת��������ƿ�У�
��5�����ݶ��ݵ���ȷ�������
��6�������������������ʵ����ʵ�������Һ�����Ӱ�죬����C=![]() ������������
������������
�⣺��1��240mL 0.4molL��1��Na2CO3��Һ��û�й��Ϊ240mL������ƿ������ʱ��Ҫѡ��250mL������ƿ��ʵ�������Ƶ���250mL 0.4mol/L��̼������Һ�����Ʋ���Ϊ�����㡢�������ܽ⡢��ȴ��ת�ơ�ϴ�ӡ����ݡ�ҡ�ȵȣ���Ҫʹ�õ������У�������ƽ�����������ձ���ҩ�ס�250mL����ƿ����ͷ�ιܵȣ���ȱ�ٵIJ�������Ϊ��250mL����ƿ����ͷ�ιܣ�
�ʴ�Ϊ��250mL����ƿ����ͷ�ιܣ�
��2������240mL 0.4molL��1��NaOH��Һ��Ӧ����250ml����Ҫ���ʵ�����=0.4molL��1��0.25L��106g/mol=10.6g��
�ʴ�Ϊ��10.6g��
��3������������Na2CO3����Ӧ����С�ձ��в�������ƽ�����̣�
�ʴ�Ϊ�����̣�
��4����ҺʱΪ��ֹҺ��������Ӧ�ò�����������ϴ���ձ�2�Ρ�3����Ϊ�˱�֤����ȫ��ת��������ƿ�У�
�ʴ�Ϊ������������֤����ȫ��ת��������ƿ�У�
��5�����ݵIJ����ǣ�������ƿ�м�������ˮ����̶���1 cm��2 cmʱ�����ý�ͷ�ιܵμ�����ˮ��Һ��İ�Һ����ʹ��Ϳ̶������У�
�ʴ�Ϊ��������ƿ�м�������ˮ����̶���1 cm��2 cmʱ�����ý�ͷ�ιܵμ�����ˮ��Һ��İ�Һ����ʹ��Ϳ̶������У�
��6��A������ʹ����ֽ����Na2CO3���壬��ʵ����Ӱ�죻
B������ƿ��ԭ��������������ˮ�������ʵ����ʵ�������Һ�����������Ӱ�죬��ҺŨ�Ȳ��䣻
C���ܽ����ձ�δ�����ϴ�ӣ���������û����ȫת�Ƶ�����ƿ��ʹŨ��ƫ�ͣ�
��ʹ������Һ�����ʵ���Ũ��ƫ�͵���C��
�ʴ�Ϊ��C��


 �¿α�ͬ��ѵ��ϵ�д�
�¿α�ͬ��ѵ��ϵ�д� һ����ʦ����Ӧ����������һ��ȫϵ�д�
һ����ʦ����Ӧ����������һ��ȫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ������ʯ�ͻ�����չˮƽ�ı�־��
A��ʯ�Ͳ��� B����ϩ���� C����Ȼ������ D�����Ͳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л����ڿ�������ȫȼ��ֻ���ɶ�����̼��ˮ������л���
A. һ��������Ԫ��
B. һ����������Ԫ��
C. һ������̼���⡢������Ԫ��
D. һ������̼��������Ԫ�أ�����ȷ���Ƿ�����Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����O2��HC1ת��ΪCl2�������Ч�棬������Ⱦ����ͳ�ϸ�ת��ͨ������ͼ��ʾ�Ĵ���ѭ��ʵ�֣�

���У���Ӧ��Ϊ��2HCl(g)+CuO(s) ![]() H2O(g)+CuCl2��s�� ��H1����Ӧ������1 mol Cl2 (g)�ķ�Ӧ��Ϊ��H2�����ܷ�Ӧ���Ȼ�ѧ����ʽΪ____________________________������Ӧ������H1����H2��ʾ����
H2O(g)+CuCl2��s�� ��H1����Ӧ������1 mol Cl2 (g)�ķ�Ӧ��Ϊ��H2�����ܷ�Ӧ���Ȼ�ѧ����ʽΪ____________________________������Ӧ������H1����H2��ʾ����
��2��һ�������²��������Ӧ������c(Cl2)���������£�
t��min�� | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
c(Cl2)/10-3(mol/L) | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
����2.0��6.0min����HCl�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���� _________��
��3�������£�����ȥ��������Ĥ��Al��CuƬ����ŨHNO3�����ԭ��أ�ͼ1�������ԭ��صĵ���ǿ�ȣ�I����ʱ�䣨t���ı仯��ͼ2��ʾ����Ӧ�������к���ɫ���������

0��tlʱ��ԭ��صĸ�����AlƬ����ʱ�������ĵ缫��Ӧʽ��______________����Һ�е�H+��______���ƶ���tlʱ��ԭ����е��������������ı䣬��ԭ����_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Դ��ͨ����ѧ��Ӧ��������( )
A. ̫����
B. ��ϫ��
C. ����
D. ����ȼ�ղ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������A��B����ѧ���������ʣ�������������ֻ�ܴӱ���ѡ��
������ | K+��Na+��Fe2+��Ba2+��NH4+��Ca2+ |
������ | OH����NO3����I����HCO3����AlO2����HSO4�� |
��1����A��B��ˮ��Һ��Ϊ��ɫ����A��ˮ��Һ��ǿ���ԣ�B��ˮ��Һ��ǿ���ԣ���Ϻ����������ϡ����İ�ɫ��������ʹʪ��ĺ�ɫʯ����ֽ����ɫ�����壮
��B�Ļ�ѧʽΪ ��
��A��B��Һ��ϼ��ȷ�Ӧ�����ӷ���ʽ ��
��2����A��ˮ��Һ��dz��ɫ��B��ˮ��Һ��ɫ������ɫ��ӦΪ��ɫ����A��ˮ��Һ�м���ϡ���������������ټ���B����Һ��ƣ���A��B��ˮ��Һ����������Ա仯����
��A�Ļ�ѧʽΪ ��
�ھ�����������������Һ��Ƶ�ԭ����������֣������ӷ���ʽ��ʾ��
�� ���� ��
������һ������֤��������Һ��Ƶ�ԭ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�������ijһ������M��N�����ʵ����淴Ӧʱ��仯����������ͼ�����б�������ȷ����
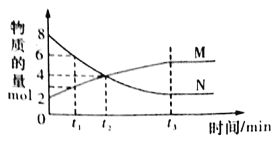
A����Ӧ�Ļ�ѧ����ʽΪ��2M![]() N
N
B��t2ʱ�����淴Ӧ������ȣ��ﵽƽ��
C��t3ʱ������Ӧ���ʴ����淴Ӧ����
D��t1ʱ��N��Ũ����MŨ�ȵ�2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��С������ͼװ����ʵ��װ��(����ͷ�ι��еĹ���������Һ�����ȣ�Ũ�ȷֱ�Ϊ5%��10%)��ʵ��ʱ��ͬʱ��ȫ������ιܵĽ�ͷ�����۲�ʵ������
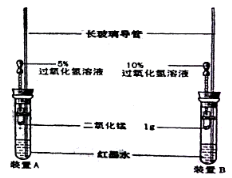
��1��С����ʵ��Ŀ���ǣ�__________________________��
��2��װ���г��������ܵ������ǣ�____________________����īˮ��������_________________��
��3��������������������е�ʵ��������____________________��������___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����������Һ��ϡH2SO4��Ӧ�����������������Na2S2O3��H2SO4===Na2SO4��S����SO2����H2O��ijͬѧ���±�����ʵ�飬�����ж���һ���ȳ��ֻ��ǡ�
��� | ��3%Na2S2O3/mL | ��1��5��H2SO4/�� | �¶�/�� |
1 | 5 | 25 | 25 |
2 | 5 | 15 | 35 |
3 | 5 | 25 | 45 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com