
【题目】实验室制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫。有人设计下图所示装置进行实验以确认上述混合气体中有乙烯和二氧化硫。试回答下列问题:

(1)图中①、②、③、④装置可盛放的试剂是(填序号):①________;②________;
③________;④________。
A.品红溶液 B.氢氧化钠溶液
C.浓硫酸 D.高锰酸钾酸性溶液
(2)能说明二氧化硫气体存在的现象是_____________________。
(3)使用装置②的目的是_________________________________。
(4)使用装置③的目的是_________________________________。
(5)确定含有乙烯的现象是_______________________________。
【答案】 A B A D ①装置中的品红溶液褪色 将SO2气体完全吸收,避免干扰乙烯性质的检验 检验SO2是否已完全被吸收 ③装置的品红溶液不褪色,④装置中的酸性KMnO4溶液褪色
【解析】二氧化硫为酸性气体,可与碱反应,可使品红褪色,具有还原性,可与酸性高锰酸钾发生氧化还原反应,而乙烯含有碳碳双键,能够与酸性高锰酸钾发生氧化还原反应,使高锰酸钾褪色,所以先检验二氧化硫,然后检验乙烯,同在检验乙烯之前用NaOH溶液除去SO2,再通过品红溶液不褪色确认SO2已除干净,最后用高锰酸钾酸性溶液褪色检验乙烯。
(1)装置①中盛有品红溶液,用来检验二氧化硫的存在;然后将气体通入盛有氢氧化钠溶液的②除去二氧化硫,再通入盛有品红溶液的③确定二氧化硫是否除干净,最后通入盛有酸性高锰酸钾的④检验乙烯的存在;故答案为:A;B;A;D;
(2)二氧化硫具有漂白性,能够使品红溶液褪色,故答案为:①中品红溶液褪色;
(3)装置②用来除去SO2气体,以免干扰乙烯的性质实验,故答案为:吸收SO2;
(4)装置③检验SO2是否被除尽,防止干扰乙烯的性质实验,故答案为:检验SO2是否被除尽;
(5)装置③中的品红溶液不退色可以排除二氧化硫的干扰,若装置④中的酸性KMnO4溶液退色,可证明乙烯的存在,故答案为:③中品红溶液不褪色,④中KMnO4溶液褪色。


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
【题目】氢氧化钠是重要的化工原料,请回答下列问题:
(一)用氢氧化钠溶液制备NaClO、NaClO3等
(1)NaOH中所含化学键类型为______________。NaClO3的化学名称为_____________。
(2)已知:Cl2(g)+2NaOH(aq)=NaCl(aq)+ NaClO(aq)+H2O(l) △H1= -102 kJ·mol-1
3Cl2(g)+6NaOH(aq)=5NaCl(aq)+ NaClO3(aq)+3H2O(l) △H2= -422 kJ·mol-1
写出在溶液中NaClO分解生成 NaClO3的热化学方程式___________________________。
(二)用氢氧化钠溶液处理天然气中少量的羰基硫(COS)及利用的过程如下(部分产物已略去):![]() .
.
(3)羰基硫与CO2结构相似,则羰基硫分子的电子式为_______________。
(4)反应I除生成两种正盐外,还有水生成,其化学方程式为__________________。
(5)已知X溶液中硫元素的主要存在形式为S2O32-,则II中主要反应的离子方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点。在一定温度下,用0.1mol/LKOH溶液分别滴定体积均为20mL、浓度均为0.1mol/L的盐酸和醋酸溶液,滴定曲线如图所示。下列有关判断正确的是
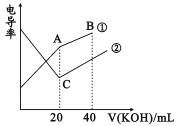
A. B点的溶液中有:c(K+)>c(OH-)>c(CH3COO-)>c(H+)
B. A点的溶液中有:c(CH3COO-)+c(OH-)-c(H+)=0.1mol/L
C. C点水电离的c(OH-)大于A点水电离的c(OH-)
D. A、B、C三点溶液均有Kw=c(H+)·c(OH-)=1.0×10-14
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别为0.6mol和0.5mol的A、B两种气体,充入0.4L密闭容器中发生反应:3A(g)+B(g) ![]() mC(g)+2D(g),经5min达到平衡,此时C为0.2mol。又知在此反应时间内D的平均反应速率为0.1mol·L-1·min-1,回答下列问题:
mC(g)+2D(g),经5min达到平衡,此时C为0.2mol。又知在此反应时间内D的平均反应速率为0.1mol·L-1·min-1,回答下列问题:
(1)m值为__________________;
(2)B的转化率为_______________________;
(3)平衡时容器内物质的总物质的量为________________________;
(4)在四种不同的条件下测定得到以下反应速率,其中表示的反应速率最快的是______
①v(A)=0.5 mol·L-1·min-1 ② v(B)=0.2 mol·L-1·min-1
③ v(C)=0.3 mol·L-1·min-1 ④ v(D)=0.1 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应A(g)+3B(s) ![]() 2C(g)+2D(g),在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
2C(g)+2D(g),在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
A. v(C)=0.1 mol·L-1·s-1 B. v(B)=l.2 mol·L-1·s-1
C. v(D)=0.4 mol·L-1·min-1 D. v(A)=0.5 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图象分别表示有关反应的反应过程与能量变化的关系,下列说法中正确的是
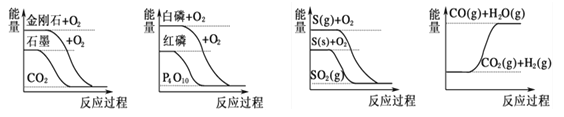
A. 石墨转变为金刚石是吸热反应
B. 相同条件下等质量S(g)比S(s)的能量低
C. 白磷比红磷稳定
D. CO(g)+H2O(g)═CO2(g)+H2(g)是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X元素的1个原子失去2个电子,被Y元素的2个原子各获得1个电子,形成离子化合物Z,下列说法中不正确的是
A. Z化学式表示为X2Y B. 固态Z熔化后能导电
C. 固态Z是离子晶体 D. X形成+2价阳离子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com