
【题目】苯乙烷(C8H10)可生产塑料单体苯乙烯(C8H8),其反应原理是C8H10(g)![]() C8H8(g)+H2(g) ΔH=+125kJ·mol-1
C8H8(g)+H2(g) ΔH=+125kJ·mol-1
Ⅰ.某温度下,将0.40mol苯乙烷,充入2L真空密闭容器中发生反应,测定不同时间该容器内物质的量,得到数据如下表:
时间/min | 0 | 10 | 20 | 30 | 40 |
n(C8H10)/mol | 0.40 | 0.30 | 0.26 | n2 | n3 |
n(C8H8)/mol | 0.00 | 0.10 | n1 | 0.16 | 0.16 |
(1)该温度下,该反应的化学平衡常数K=________________。
(2)若保持其他条件不变,用0.40molH2(g)和0.40molC8H8(g)合成C8H10(g),当有30kJ热量放出时,该反应中H2的转化率是________________,通过计算说明此时,该反应是否达到了平衡状态__________?
【答案】![]() 60% Q=
60% Q=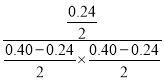 =
=![]() =
=![]() ,所以处于平衡状态
,所以处于平衡状态
【解析】
计算反应C8H10(g)C8H8(g)+H2(g)的化学平衡常数,需先求出平衡时各物质的浓度,然后代入公式K=![]() 进行计算;对于反应C8H8(g)+H2(g)
进行计算;对于反应C8H8(g)+H2(g)![]() C8H10(g) ΔH=-125kJ·mol-1,由放热30kJ,可计算出参加反应的H2的物质的量,由此可求出转化率;并利用浓度求出浓度商;此反应的平衡常数与反应C8H10(g)
C8H10(g) ΔH=-125kJ·mol-1,由放热30kJ,可计算出参加反应的H2的物质的量,由此可求出转化率;并利用浓度求出浓度商;此反应的平衡常数与反应C8H10(g)![]() C8H8(g)+H2(g)的平衡常数互为倒数,比较浓度商与平衡常数,便可得出结论。
C8H8(g)+H2(g)的平衡常数互为倒数,比较浓度商与平衡常数,便可得出结论。
(1)利用表中数据,可建立如下三段式:
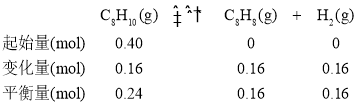
该温度下,该反应的化学平衡常数K=![]() =
=![]() 。答案为:
。答案为:![]() ;
;
(2)对于反应C8H8(g)+H2(g)![]() C8H10(g) ΔH=-125kJ·mol-1,当放热30kJ时,参加反应的H2的物质的量为
C8H10(g) ΔH=-125kJ·mol-1,当放热30kJ时,参加反应的H2的物质的量为![]() =0.24mol,则该反应中H2的转化率是
=0.24mol,则该反应中H2的转化率是![]() =60%;从而得出参加反应的的C8H8物质的量为0.24mol,生成C8H10的物质的量为0.24mol,浓度商Q=
=60%;从而得出参加反应的的C8H8物质的量为0.24mol,生成C8H10的物质的量为0.24mol,浓度商Q=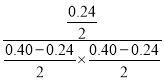 =
=![]() =
=![]() ,所以处于平衡状态。答案为:60%;Q=
,所以处于平衡状态。答案为:60%;Q=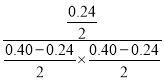 =
=![]() =
=![]() ,所以处于平衡状态。
,所以处于平衡状态。


科目:高中化学 来源: 题型:
【题目】钴的合金及其配合物用途非常广泛。
(1) Co3+基态核外电子排布式为________。
(2) 一种Pt、Co金属间化合物可作为质子交换膜燃料电池的催化剂,其晶胞结构如图所示,该金属间化合物的化学式为________。

(3) BNCP可用于激光起爆器等,BNCP可由HClO4、CTCN、NaNT共反应制备。
①ClO4-的空间构型为________ (用文字描述)。
②CTCN的化学式为[Co(NH3)4CO3]NO3,与Co(Ⅲ)形成配位键的原子是________ (已知CO32-的结构式为![]() )。
)。
③NaNT可由![]() (双聚氰胺)为原料制备。双聚氰胺中碳原子杂化轨道类型为________,1 mol该分子中含σ键的数目为________。
(双聚氰胺)为原料制备。双聚氰胺中碳原子杂化轨道类型为________,1 mol该分子中含σ键的数目为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是![]()
A.检验稀盐酸和氢氧化钠溶液是否恰好完全反应,可在反应后溶液中滴加无色酚酞溶液,无明显现象,恰好完全反应
B.某液体可能是海水或蒸馏水,将其蒸发结晶,液体消失,无残留物,该液体为蒸馏水
C.某溶液完全蒸发后无固体残留物,该溶液中一定含硫酸根离子
D.某溶液中加入稀盐酸有气泡产生,该溶液中一定含碳酸根离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的工业硫酸盐废水中含有大量的Fe2+、Fe3+、较多的Cu2+和少量的Na+。工厂计划从该废水中回收硫酸亚铁和金属铜,设计如下流程图。
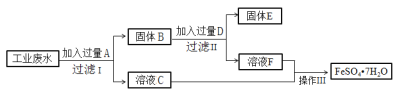
回答下列问题;
(1)A的化学式为_________,D的化学式为_______。
(2)在工业废水中加入过量A时,发应的离子方程式有:___________、__________。
(3)得到FeSO47H2O晶体的操作Ⅲ为:加热浓缩、冷却结晶、______、______、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出以下实验的实验现象:
(1)向盛有FeCl3溶液的试管中加入KSCN溶液。____
(2)将密封有NO2的玻璃球浸泡在热水中。________
(3)向酸性高锰酸钾溶液中加入草酸溶液。______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于吸热反应的是______(填字母)。
A.Na2O与水反应 B.甲烷的燃烧反应C.CaCO3受热分解 D.锌与盐酸反应
(2)获取能量变化的途径① 通过化学键的键能计算。已知:
化学键种类 | H—H | O=O | O—H |
键能(kJ/mol) | 436 | 498 | 463.4 |
计算可得:2H2(g)+ O2(g) =2H2O(g) H=____________kJ·mol-1
②通过盖斯定律可计算。已知在25℃、101kPa时:
Ⅰ.2Na(s)+![]() O2(g) =Na2O(s)△H=-414kJ·mol-1
O2(g) =Na2O(s)△H=-414kJ·mol-1
Ⅱ.2Na(s)+O2(g) =Na2O2(s)△H=-511kJ·mol-1
写出Na2O2与Na反应生成Na2O的热化学方程式__________。
③ 利用实验装置测量。测量盐酸与NaOH溶液反应的热量变化的过程中,若取50 mL 0.50 mol·L-1的盐酸,则还需加入________(填序号)。
A.50 mL 0.50 mol·L-1NaOH溶液B.50 mL 0.55 mol·L-1NaOH溶液 C.1.0 g NaOH固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验操作的说法正确的是![]()
A.蒸馏操作时,应使温度计水银球伸入蒸馏烧瓶液面下
B.铂丝蘸取试样灼烧,火焰呈黄色,则该试样一定是钠盐
C.测定溶液的pH的规范操作是:用干燥洁净的玻璃棒蘸取溶液,点在pH试纸中央,跟标准比色卡比较
D.分液时,分液漏斗下层液体先从下口放出,然后将上层液体放出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 下列过程中不一定释放能量的是 ______
下列过程中不一定释放能量的是 ______ ![]() 请填编号
请填编号![]()
A 形成化学键,![]() 燃料燃烧,
燃料燃烧,![]() 化合反应,
化合反应,![]() 葡萄糖在体内的氧化分解,
葡萄糖在体内的氧化分解,![]() 酸碱中和,
酸碱中和,![]() 炸药爆炸.
炸药爆炸.
![]() 已知A和B是同种元素的两种单质,A转化为B时需放出能量,则A和B相比较而言,较稳定的是 ______
已知A和B是同种元素的两种单质,A转化为B时需放出能量,则A和B相比较而言,较稳定的是 ______ ![]() 请填A或
请填A或![]() .
.
![]() 在
在![]() C、
C、![]() C、
C、![]() 、
、![]() 几种核素中,互称为同位素的是 ______
几种核素中,互称为同位素的是 ______
![]() 下列五种有机物中:
下列五种有机物中:![]()
![]()
![]()
![]()
![]() 淀粉,
淀粉,
水溶液显酸性的是 ______ ![]() 填编号
填编号![]() .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某密闭容器中发生如下反应:X(g)+3Y(g)2Z(g);△H<0.上图表示该反应的速率(v)随时间
(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中不正确的是( )

A. ![]() 时加入了催化剂B.
时加入了催化剂B. ![]() 时降低了温度
时降低了温度
C. ![]() 时增大了压强D.
时增大了压强D. ![]() 时间内转化率最高
时间内转化率最高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com