
LiFePO4新型锂离子动力电池以其独特的优势成为奥运会绿色能的新宠。已知该电池放电时的电极反应式为:正极 FePO4+Li++e-==LiFePO4 负极 Li-e-== Li+下列说法中正确的是
A.充电时电池反应为FePO4+Li = LiFePO4
B.充电时动力电池上标注“+”的电极应与外接电的正极相连
C.放电时电池内部Li+向负极移动
D.放电时,在正极上是Li+得电子被还原
科目:高中化学 来源:2013-2014福建省南平市毕业班质量检查理综化学试卷(解析版) 题型:推断题
(13分)没食子酸丙酯简称PG,结构简式为 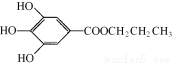 ,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂。
,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂。
⑴PG的分子式为 ,请写出PG分子中所含官能团的名称 ,1molPG与足量氢氧化钠溶液完全反应时,消耗的氢氧化钠的物质的量是 。
PG可发生如下转化:
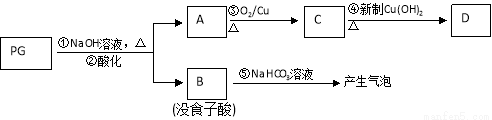
⑵A的结构简式为 ,1mol没食子酸最多可与 mol H2 加成。
⑶上图的有关变化中,属于氧化反应的有(填序号) 。
⑷从分子结构或性质上看,PG具有抗氧化作用的主要原因是(填序号) 。
A.含有苯环 B.含有羧基 C.含有酚羟基 D. 微溶于食用油
⑸反应④的化学方程式为:
⑹B有多种同分异构体,写出其中符合下列要求的同分异构体的结构简式:
i.含有苯环,且苯环上的一溴代物只有一种;ii.既能发生银镜反应,又能发生水解反应。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高一下学期期末考试化学试卷(解析版) 题型:填空题
⑴衣服上沾有动、植物油污,用水洗不掉,但可用汽油洗去,这是因为大多数有机物难溶于
而易溶于 。有机化工厂附近严禁火种,这是因为绝大多数有机物 。
(2)聚氯乙烯是一种 (填“有”或“无”)毒塑料,工业上用乙炔(CH≡CH)和氯化氢在催化剂作用下发生反应制取氯乙烯,氯乙烯再经过 反应制取聚氯乙烯。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高一下学期期末考试化学试卷(解析版) 题型:选择题
四种主族元素的离子a Xm+,bYn+,cZn-和dRm-(a,b,c,d为元素的原子序数),它们具有相同的电子层结构,若m>n,对下列叙述的判断正确的是( )
①a-b=n-m ②元素的原子序数a>b>c>d
③元素非金属性Z>R ④最高价氧化物对应水化物碱性X>Y
A.②③正确 B.只有③正确 C.①②③④正确 D.①②③正确
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省三明市三校高三下学期联考理综化学试卷(解析版) 题型:计算题
( 13分)下面的表格是元素周期表的一部分,其中的字母对应不同的元素。
A |
|
| |||||||||||||||
|
|
|
| M | Q | R |
|
| |||||||||
|
| E |
|
|
| D |
| ||||||||||
|
|
| G |
|
|
| J |
|
|
|
|
|
|
|
|
|
|
请回答下列问题:
(1)G和J形成的合金是一种贮氢材料,其晶体结构与氯化铯相同。该合金中每个G原子周围与其最近且等距的J原子有 个。该晶体属于 晶体
A .离子晶体 B . 原子晶体 C . 分子晶体 D. 金属晶体
(2)M3R2是一种直线型分子R=M=M=M=R,该分子是一种 分子(填极性或非极性)。
(3)请写出D-的电子排布式: 。
(4)M2A2也是直线型分子,1个分子中含有 个σ键。
(5)化合物E2D6分子中各原子均达到了八电子稳定结构,请画出其结构式。(用元素符号表示)
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省“四地六校”下学期第三次联考高二化学试卷(解析版) 题型:填空题
(7分)决定物质性质的重要因素是物质结构。请回答下列问题:
(1)铜是过渡元素。化合物中,铜常呈现+1价或+2价。右图为某铜氧化物晶体结构单元,该氧化物的化学式为 。
(2)第三周期部分元素氟化物的熔点见下表:
氟化物 | NaF | MgF2 | SiF4 |
熔点/K | 1266 | 1534 | 183 |
解释MgF2与SiF4熔点差异的原因 。
(3)A和B为第三周期元素,其原子的部分电离能如下表所示:
电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
A | 578 | 1817 | 2745 | 11578 |
B | 738 | 1451 | 7733 | 10540 |
则A的电负性 B的电负性(填“>”、“<”或“=”)。
(4)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5、CrO2、Fe3O4中,更适合作录音带磁粉原料的是__________(填化学式)。
(5)实验室检验Ni2+可用丁二酮肟与之作用生成腥红色配合物沉淀。
②在配合物中用化学键和氢键标出未画出的作用力(镍的配位数为4)。
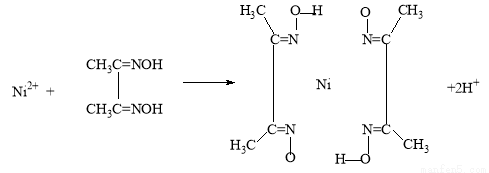
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省“四地六校”下学期第三次联考高二化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中能大量共存的是( )
A.pH=1的溶液中:Na+、Fe2+、NO3-、SO42-
B.滴入酚酞试液显红色的溶液中:K+、Fe3+、ClO-、SO42-
C.c(H+)/c(OH-)=1×1012的溶液中:NH4-、Cl-、NO3-、Al3+
D.由水电离出的c(H+)=1×10-12mol/L的溶液中:Na+、K+、Cl-、HCO3-
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省“四地六校”下学期第三次联考高一化学试卷(解析版) 题型:填空题
根据元素周期表1~20号元素的性质和递变规律,回答下列问题。
(1)属于金属元素的有____种,金属性最强的元素与氧气反应生成的化合物有______________(至少填两种化合物的化学式);
(2)属于稀有气体的是_________(填元素符号,下同);
(3)形成化合物种类最多的两种元素是__________________;
(4)第三周期中,原子半径最大的是(稀有气体除外)____________;
(5)推测Si、N最简单氢化物的稳定性由强到弱排列_____________(填化学式)。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建安溪一中、惠安一中、养正中学下学期期中高二化学(解析版) 题型:选择题
“摇摇冰”是一种即用即冷的饮料。吸食时将饮料罐隔离层中的化学物质和水混合后摇动即可制冷。该化学物质是 ( )
A. 氯化钠 B. 固体硝酸铵 C. 固体氢氧化钠 D. 生石灰
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com