

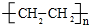 ;
;分析 (1)浓硫酸增重5.4g为生成水的质量,物质的量为0.3mol,碱石灰增重8.8g克为生成二氧化碳的质量,物质的量为0.2mol,根据氧原子守恒可知有机物中含n(O)=0.2mol×2+0.3mol-0.6mol=0.1mol,则有机物的最简式为C2H6O;
(2)质谱仪测定有机化合物的相对分子质量为46,结合最简式判断分子式为C2H6O;
(3)A可能为乙醇或二甲醚;
(4)有机物A分子中有三种不同化学环境的氢原子,应为乙醇,二甲醚只有一种不同化学环境的氢原子;
(5)A在一定条件下脱水可生成B,B为CH2=CH2,B可合成包装塑料C,C为聚乙烯;
(6)原子利用率为100%,可用加成方法制备,乙烯与HCl发生加成反应生成氯乙烷.
解答 解:(1)n(CO2)=$\frac{8.8g}{44g/mol}$=0.2mol,n(H2O)=$\frac{5.4g}{18g/mol}$=0.3mol,n(O2)=$\frac{6.72L}{22.4L/mol}$=0.3mol,则有机物中含n(O)=0.2mol×2+0.3mol-0.6mol=0.1mol,则有机物中N(C):N(H):N(O)=0.2mol:0.6mol:0.1mol=2:6:1,最简式为C2H6O,
故答案为:C2H6O;
(2)最简式为C2H6O,有机化合物的相对分子质量为46,则该物质的分子式是C2H6O,
故答案为:46;C2H6O;
(3)A可能为乙醇或二甲醚,结构简式为CH3CH2OH、CH3-O-CH3,
故答案为:CH3CH2OH、CH3-O-CH3;
(4)有机物A分子中有三种不同化学环境的氢原子,应为乙醇,即CH3CH2OH,二甲醚只有一种不同化学环境的氢原子,
故答案为:CH3CH2OH;
(5)A在一定条件下脱水可生成B,B为CH2=CH2,B可合成包装塑料C,C为聚乙烯,B转化为C的化学反应方程式为:nCH2=CH2$\stackrel{催化剂}{→}$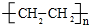 ,
,
故答案为:nCH2=CH2$\stackrel{催化剂}{→}$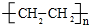 ;
;
(6)原子利用率为100%,可用加成方法制备,乙烯与HCl发生加成反应生成氯乙烷,反应的方程式为:CH2=CH2 +HCl $\stackrel{催化剂}{→}$CH3CH2 Cl,
故答案为:CH2=CH2 +HCl $\stackrel{催化剂}{→}$CH3CH2 Cl.
点评 本题考查有机物结构式的确定,掌握燃烧法利用原子守恒前后有机物分子,对质谱图、核磁共振氢谱、红外光谱图进行简单识读.


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12.0 g熔融的NaHSO4中含有离子总数为0.2NA | |
| B. | 电解精炼Cu时,导线中通过2NAe-时,阳极质量减少64 g | |
| C. | 标准状况下,11.2 LCHCl3中含有的共用电子对数目为2NA | |
| D. | 标准状况下,0.1 mol Cl2溶于水,转移的电子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
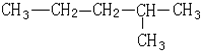
| A. | 该有机物属于烷烃 | |
| B. | 该烃与2,3-二甲基丁烷互为同系物 | |
| C. | 该烃的一氯取代产物共有5种 | |
| D. | 该有机物可由两种单炔烃分别与氢气加成得到 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷与氯气混合后光照发生反应 | B. | 乙炔与氯气的加成反应 | ||
| C. | 乙烯与氯化氢的加成反应 | D. | 二氧化碳通入石灰水中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com