
【题目】已知:乙二酸(HOOC—COOH,可简写为H2C2O4),俗称草酸,157℃时开始分解。
(1)探究草酸的酸性
25℃ H2C2O4 K1=5.4×10-2,K2=5.4×10-5;H2CO3 K1=4.5×10-7,K2=4.7×10-11
下列化学方程式可能正确的是___。
A.H2C2O4+![]() =
=![]() +
+![]() B.
B.![]() +
+![]() =
=![]() +
+![]()
C.2![]() +CO2+H2O=2
+CO2+H2O=2![]() +
+![]() D.H2C2O4+
D.H2C2O4+![]() =
=![]() +H2O+CO2↑
+H2O+CO2↑
(2)探究草酸分解产物
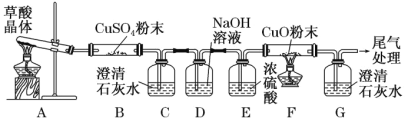
实验中观察到 B 中 CuSO4 粉末变蓝,C 中澄清石灰水变浑浊,D 的作用是 ___, 证明有 CO 气体生成的现象是______。
(3)探究催化剂对化学反应速率的影响
在甲、乙两支试管中各加入 4 mL 0.01 mol·L-1 酸性 KMnO4 溶液和 2 mL 0.1 mol·L-1H2C2O4 溶液,再向乙试管中加入一粒黄豆大的 MnSO4 固体,摇匀。填写表格:
反应现象 | ①_______ |
实验结论 | ②______ |
试管中发生反应的离子方程式 | ③______ |
(4)用酸性 KMnO4 溶液滴定 Na2C2O4,求算 Na2C2O4 的纯度。
实验步骤:准确称取 2.0 g Na2C2O4 固体,配成 100 mL 溶液;取出 20.00 mL 于锥形瓶
①KMnO4 溶液应装在_________ 滴定管中。(填“酸式”或“碱式”)
②Na2C2O4 的纯度是_________。
【答案】BD 吸收CO2气体 F中黑色CuO变成光亮的红色,G中澄清石灰水变浑浊 两支试管中紫色KMnO4溶液均褪色,乙试管中溶液褪色较快 MnSO4(Mn2+)是此反应的催化剂,加入催化剂可以使化学反应速率加快 2![]() +5H2C2O4+6H+=10CO2↑+2Mn2++8H2O 酸式 33.5%
+5H2C2O4+6H+=10CO2↑+2Mn2++8H2O 酸式 33.5%
【解析】
(1)电离常数越大其酸性越强,根据强酸制取弱酸判断;
(2)氢氧化钠是碱能吸收酸性氧化物;一氧化碳具有还原性,二氧化碳能使澄清石灰水变浑浊;
(3)高锰酸钾具有氧化性,能氧化还原性物质,硫酸锰具有催化作用,加快反应速率;
(4)①酸式滴定管能量取酸性溶液;
②根据高锰酸钾计算草酸钠的纯度。H2C2O4+![]() =
=![]() +
+![]()
(1)根据电离常数知酸性强弱顺序是:H2C2O4>![]() >H2CO3>
>H2CO3>![]() ,根据强酸制取弱酸知草酸和碳酸根离子反应生成草酸根离子和二氧化碳,草酸氢根离子和碳酸根离子反应生成碳酸氢根离子和草酸根离子,故选BD;
,根据强酸制取弱酸知草酸和碳酸根离子反应生成草酸根离子和二氧化碳,草酸氢根离子和碳酸根离子反应生成碳酸氢根离子和草酸根离子,故选BD;
(2)氢氧化钠是强碱能吸收酸性氧化物二氧化碳,一氧化碳具有还原性,能还原黑色的氧化铜生成红色的铜,同时自身被氧化生成二氧化碳,二氧化碳使澄清的石灰水变浑浊,所以看到的现象是:F中黑色CuO变成光亮的红色,G中澄清石灰水变浑浊,
故答案为:吸收CO2气体;F中黑色CuO变成光亮的红色,G中澄清石灰水变浑浊;
(3)看到的现象是两支试管中紫色KMnO4溶液均褪色,乙试管中溶液褪色较快;通过对比实验知,硫酸锰是该反应的催化剂,加入催化剂能加快反应速率;该反应中高锰酸根离子被还原生成锰离子,草酸被氧化生成二氧化碳,离子反应方程式为:2![]() +5H2C2O4+6H+=10CO2↑+2Mn2++8H2O;
+5H2C2O4+6H+=10CO2↑+2Mn2++8H2O;
故答案为:两支试管中紫色KMnO4溶液均褪色,乙试管中溶液褪色较快;MnSO4(Mn2+)是此反应的催化剂,加入催化剂可以使化学反应速率加快;2![]() +5H2C2O4+6H+=10CO2↑+2Mn2++8H2O;
+5H2C2O4+6H+=10CO2↑+2Mn2++8H2O;
(4)①高锰酸钾溶液呈酸性且具有强氧化性,易腐蚀橡胶,应该用酸式滴定管量取,故答案为:酸式;
②设草酸钠的质量分数为x,

x=![]() ×100%=33.5%,
×100%=33.5%,
答:草酸钠的质量分数为33.5%。
故答案为:33.5%;


科目:高中化学 来源: 题型:
【题目】合成氨是人类科学技术上的一项重大突破,是化学和技术对社会发展与进步的巨大贡献之一。在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学反应方程式(HAc表示醋酸):Cu(NH3)2Ac + CO + NH3Cu(NH3)3(CO)Ac。请回答下列问题:
(1)C、N、O的第一电离能由大到小的顺序为________。
(2)写出基态Cu+的核外电子排布式_______。
(3)配合物Cu(NH3)3(CO)Ac中心原子的配位数为______。
(4)写出与CO互为等电子体的阴离子______。(任写一个)
(5)在一定条件下NH3与CO2能合成化肥尿素[CO(NH2)2],1mol尿素分子中,σ键的数目为______。
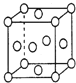
(6)已知铜的晶胞结构如图所示,则在铜的晶胞中所含铜原子数及配位数比为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿司匹林是一种常见药物,它的相对分子质量为180,含C、H、O三种元素,其中含C、H的质量分数分别为60%、4.4%,则阿司匹林的分子式是( )
A.C10H9O4B.C10H22O3C.C9H10O4D.C9H8O4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)按要求书写下列物质的系统命名:
①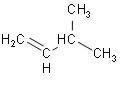 ,将其在催化剂存在下完全与氢气加成所得的产物____;
,将其在催化剂存在下完全与氢气加成所得的产物____;
②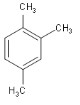 ____。
____。
(2)书写下列物质的结构简式:
①分子式为C5H10的烃存在顺反异构,写出它的顺反两种异构体的结构简式:_____;
②分子式为C9H12的芳香烃,苯环上的一溴取代物只有一种,写出该芳香烃的结构简式:_____。
(3)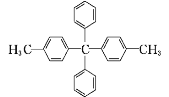 共线的碳原子最多有____个。
共线的碳原子最多有____个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在氮及其化合物的化工生产中,对有关反应的反应原理进行研究有着重要意义。
(1)t℃时,关于N2、NH3的两个反应的信息如下表所示:
化学反应 | 正反应活化能 | 逆反应活化能 | t℃时平衡常数 |
N2(g)+O2(g)=2NO(g) △H>0 | a kJ/mol | b kJ/mol | K1 |
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H<0 | c kJ/mol | d kJ/mol | K2 |
请写出t℃时氨气被一氧化氮氧化生成无毒气体的热化学方程式:______________________,t℃时该反应的平衡常数为__________ (用K1和K2表示)。
(2)工业合成氨的原理为:N2(g)+3H2(g)![]() 2NH3(g)下图甲表示在一定体积的密闭容器中反应时,H2的物质的量浓度随时间的变化。图乙表示在其他条件不变的情况下,起始投料H2与N2的物质的量之比(设为x)与平衡时NH3的物质的量分数的关系。
2NH3(g)下图甲表示在一定体积的密闭容器中反应时,H2的物质的量浓度随时间的变化。图乙表示在其他条件不变的情况下,起始投料H2与N2的物质的量之比(设为x)与平衡时NH3的物质的量分数的关系。

①图甲中0~t1 min内,v(N2)=_____mol·L-1·min-1;b点的v(H2)正_____a点的v(H2)逆(填“大于”“小于”或“等于”)。
②己知某温度下该反应达平衡时各物质均为1 mol,容器体积为1L,保持温度和压强不变,又充入3 mol N2后,平衡________(填“向右移动”“向左移动”或“不移动”)。
(3)①科学家研究出以尿素为动力的燃料电池新技术。用这种电池可直接去除城市废水中的尿素,既能产生净化的水,又能发电。尿素燃料电池结构如图所示,写出负极电极反应式:________________________________________________。
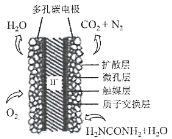
②理论上电池工作时,每消耗标准状况下2.24 L O2时,可产生的电量为________ (法拉第常数为96500C/ mol)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中有![]() 、Mg2+ 和Fe2+ 三种离子,若向其中加入过量的NaOH溶液,微热并搅拌,再加入过量的盐酸,溶液中大量减少的阳离子是
、Mg2+ 和Fe2+ 三种离子,若向其中加入过量的NaOH溶液,微热并搅拌,再加入过量的盐酸,溶液中大量减少的阳离子是
A.只有![]() B.Mg2+ 、Fe2+C.
B.Mg2+ 、Fe2+C.![]() 、Fe2+D.全部
、Fe2+D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体胃酸的主要成分是盐酸。胃酸可助消化食物,但胃酸过多会损伤胃粘膜,使人感觉不适。抗酸药(又称抑酸剂)可以减少过多的胃酸。下列物质不属于抗酸药的是
A.胃得乐(主要成分:MgCO3)B.胃舒平[主要成分:Al(OH)3]
C.碳酸氢钠片(主要成分:NaHCO3)D.阿司匹林(主要成分: ![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: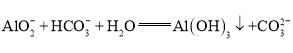 。向含0.01 mol
。向含0.01 mol ![]() 和0.02 mol NaOH的稀溶液中缓慢通入CO2,溶液中,
和0.02 mol NaOH的稀溶液中缓慢通入CO2,溶液中,![]() 随通入的
随通入的![]() 的变化如图,下列对应关系正确的是( )
的变化如图,下列对应关系正确的是( )
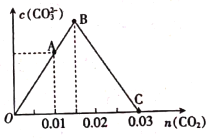
A.A点:![]()
B.B点:![]()
C.C点:![]()
D.O点:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PMMA是一种具有较好的透明性、化学稳定性、易染色、易加工、外观优美的塑料,在建筑业中有着广泛应用,分子式是![]() 。一种从原料
。一种从原料![]() 合成PMMA的路线如图所示:
合成PMMA的路线如图所示:
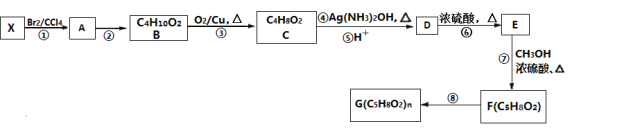
请回答:
(1)原料X的结构简式为________。
(2)②的反应类型是________。F中含有的官能团名称是________。
(3)写出④的化学方程式________。
(4)D的同分异构体中,能发生银镜反应、水解反应和酯化反应的同分异构体有________种。
(5)已知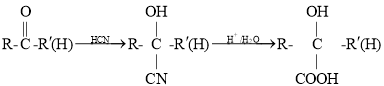 (其中R、
(其中R、![]() 均代表烃基)。若以丙烯为原料,利用上述信息设计合成中间体D,在得到D的同时也得到了另一种有机副产物M,则M可能的结构简式是________。
均代表烃基)。若以丙烯为原料,利用上述信息设计合成中间体D,在得到D的同时也得到了另一种有机副产物M,则M可能的结构简式是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com