
【题目】甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间的转化关系如图所示。下列有关物质的推断正确的是( )
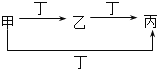
甲 | 乙 | 丙 | 丁 | |
A | S | SO2 | SO3 | O2 |
B | CO32- | HCO3- | CO2 | H+ |
C | Cl2 | FeCl3 | FeCl2 | Fe |
D | Al3+ | Al(OH)3 | AlO2- | NH3H2O |
A.AB.BC.CD.D
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应A(g)+xB(g) ![]() 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间的变化如下图所示。下列说法中正确是
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间的变化如下图所示。下列说法中正确是
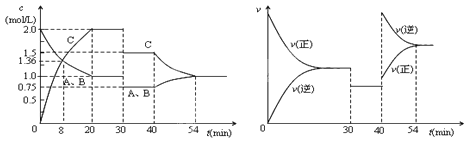
A.前8min A的平均反应速率为0.08mol/(L·s)
B.30min时扩大容器的体积,40min时升高温度
C.反应方程式中的x=1,正反应为吸热反应
D.30min和54min的反应的平衡常数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,回答下列问题:
(1)在鼓泡反应器中通入含有SO2和NOx的烟气,反应温度为323K,NaClO2碱性溶液浓度为5×103mol·L1。反应一段时间后溶液中离子浓度的分析结果如表。
离子 | SO42 | SO32 | NO3 | NO2 | Cl |
c/mol·L1 | 8.35×104 | 6.87×106 | 1.5×104 | 1.2×105 | 3.4×103 |
①写出NaClO2碱性溶液脱硝(NO)过程中主要反应的离子方程式:____。增加压强,NO的转化率___(填“提高”“不变”或“降低”)
②由实验结果可知,脱硫反应速率大于脱硝反应速率,原因是除了SO2和NO在烟气中的初始浓度不同,还可能是___。
(2)在不同温度下,NaClO2溶液脱硫、脱硝的反应中,SO2和NO的平衡分压px如图所示。
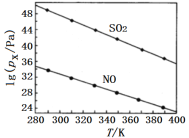
由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均___(填“增大”“不变”或“减小”)。
(3)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)苏丹红颜色鲜艳、价格低廉,常被一些企业非法作为食品和化妆品等的染色剂,严重危害人们健康。苏丹红常见有Ⅰ、Ⅱ、Ⅲ、Ⅳ4种类型,苏丹红Ⅰ的分子结构如图1所示。
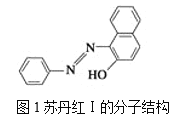
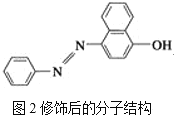
苏丹红Ⅰ在水中的溶解度很小,微溶于乙醇,有人把羟基取代在对位形成图2所示的结构,则其在水中的溶解度会____(填“增大”或“减小”),原因是__________________。
(2)Co(NH3)5BrSO4可形成两种钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀;在第二种配合物溶液中加入BaCl2溶液时,则无明显现象,则第一种配合物的结构式为__________,第二种配合物的结构式为_____。
(3)Ag+能与NH3、S2O32-、CN等形成配位数为2的配合物。
利用AgNO3和氨水可配制[Ag(NH3)2]OH溶液,在[Ag(NH3)2]OH中存在的化学键的类型有_____(填字母)。
A 离子键 B 金属键 C 配位键 D 非极性键 E 极性键
(4)NO3-中N原子的杂化轨道类型是____,空间构型为_____。写出一种与NO2-,SO2互为等电子体的短周期元素单质分子的化学式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼化钒(VB2)—空气电池是目前储电能力最高的电池,电池示意图:
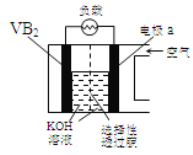
该电池工作时反应为:4VB2+ 11O2 = 4B2O3+ 2V2O5。下列说法正确的是
A.VB2极发生的电极反应为:2VB2+ 22OH-22e=V2O5+ 2B2O3+ 11H2O
B.电极a为电池负极
C.电流由VB2极经负载流向电极a
D.图中选择性透过膜允许阳离子选择性透过
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃烧法是确定有机物分子式常用的方法:在电炉加热时用纯O2氧化管内样品,根据产物的质量确定有机物的组成。若实验中所取样品A只含C、H、O三种元素中的两种或三种,准确称取0.92 g样品,经充分反应后,测得生成1.76 gCO2和1.08 g水;回答下列问题:
(1)样品A的实验式为____________。能否根据A的实验式确定A的分子式_______ (填“能”或“不能”),若能,则A的分子式是____________________ (若不能,则此空不填)。
(2)样品A不能与金属钠反应,则其结构简式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知气态烃A在标准状况下的密度是1.16 g·L1,B的产量可以用来衡量一个国家石油化工发展水平,G是一种高分子化合物。现有 A、B、C、D、E、F、G 存在如下关系:
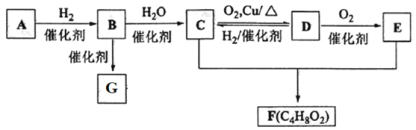
请回答:
(1)D中的官能团名称是_______________。 B的结构式为_________;
(2)写出 C+E→F反应的化学方程式__________;
(3)写出 C→D反应的化学方程式为__________;
(4)已知三分子 A 在一定条件下可合成不能使酸性 KMnO4 溶液褪色的有机物,写出该合成反应的化学方程式___________,反应类型为___________。
(5)下列有关叙述正确的是_____________。
a. A、B、C、D、E、F、G均为非电解质
b. A中所有原子不可能处于同一平面上
c. 加热时,D 能与新制氢氧化铜悬浊液反应生成砖红色沉淀
d.75%(体积分数)的 C 水溶液常用于医疗消毒
e. 将绿豆大小的钠块投入 C 中,钠块浮于液面上,并有大量气泡产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均为有机物,其中A是化学实验中常见的有机物,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平,有关物质的转化关系如图甲所示:
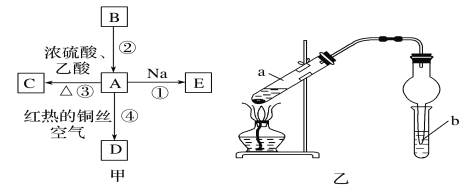
(1)C的结构简式__;A中官能团的名称为__。
(2)写出下列反应的化学方程式:
反应①__;
反应④__。
(3)实验室利用反应③制取C,常用图乙装置:
①a试管中主要反应的化学方程式为__。反应类型是__。
②在实验中用到了:铁架台(铁夹),酒精灯,试管,导管(橡胶管)和__。(填仪器名称)
③试管b中溶液名称为__,实验后观察到的现象是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾天气严重影响人们的生活和健康。因此采取改善能源结构、机动车限号等措施来减少PM2.5、SO2、NOx等污染。请回答下列问题:
Ⅰ. 臭氧是理想的烟气脱硝剂,其脱硝的反应之一为:2NO2(g)+O3(g)![]() N2O5(g)+O2(g),不同温度下,在两个恒容容器中发生该反应,相关信息如下表及图所示,回答下列问题:
N2O5(g)+O2(g),不同温度下,在两个恒容容器中发生该反应,相关信息如下表及图所示,回答下列问题:
容器 | 甲 | 乙 |
容积/L | 1 | 1 |
温度/K | T1 | T2 |
起始充入量 | 1molO3和2molNO2 | 1molO3和2molNO2 |
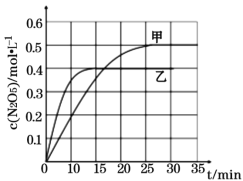
①0~15min内乙容器中反应的平均速率:v(NO2) =____(计算结果保留两位小数)。
②该反应的正反应为____(填“吸热”或“放热”)反应。
③T1时平衡后,向恒容容器中再充入1molO3和2molNO2,再次平衡后,NO2的百分含量将____(填“增大”“减小”或“不变”)。
④反应体系在温度为T1时的平衡常数为____。
⑤在恒温恒容条件下,下列条件不能证明该反应已经达到平衡的是____。
a.容器内混合气体压强不再改变
b.消耗2n molNO2的同时,消耗了n molO3
c.混合气体的平均相对分子质量不再改变
d.混合气体密度不再改变
II. 某化学小组查阅资料后得知:2NO(g)+O2(g) ![]() 2NO2(g) 的反应历程分两步:
2NO2(g) 的反应历程分两步:
①2NO(g)=N2O2(g) (快) v1正=k1正·c2(NO),v1逆=k1逆·c(N2O2)
②N2O2(g)+O2(g)=2NO2(g) (慢) v2正=k2正·c(N2O2)·c(O2),v2逆=k2逆·c2(NO2)
请回答下列问题:
(1)已知决定2NO(g)+O2(g) ![]() 2NO2(g)反应速率的是反应②,则反应①的活化能E1与反应②的活化能E2的大小关系为E1____E2(填“>”“<”或“=”)。
2NO2(g)反应速率的是反应②,则反应①的活化能E1与反应②的活化能E2的大小关系为E1____E2(填“>”“<”或“=”)。
(2)一定温度下,反应2NO(g)+O2(g) ![]() 2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=____。
2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com