
136C与147N具有相同的( )
|
| A. | 质子数 | B. | 中子数 | C. | 电子数 | D. | 质量数 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
可作为可逆反应 N2(g)+O2(g) 2NO(g)已达到平衡状态的标志的是( )
2NO(g)已达到平衡状态的标志的是( )
A.单位时间内每生成 n mol N2,同时生成2 n mol NO
B.容器内反应混合物的总压强不随时间改变
C.O2的消耗速率等于NO的消耗速率
D.容器内始终有N2、O2和NO共存
查看答案和解析>>
科目:高中化学 来源: 题型:
用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U形管)构成一个原电池。以下有关该原电池的叙述正确的是
①在外电路中,电流由铜电极流向银电极
②正极反应为:Ag++e- =Ag
③实验过程中取出盐桥,原电池仍继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
A.①② B.②③ C.②④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
废物回收利用可实现资再生,并减少污染。如废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末,废旧玻璃也可回收再生。
(1)下列处理印刷电路板非金属粉末的方法中,不符合环境保护理念的是 (填字母)。
A.热裂解形成燃油 B.露天焚烧
C.作为有机复合建筑材料的原料 D.直接填埋
(2)用H2O2和H2SO4(ag)的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(s)+2H+(aq) ====Cu2+(aq)+H2(g) ΔH=-64.39kJ·mol-1
2H2O2(l) ====2H2O (l)+O2(g) ΔH=-196.46kJ·mol-1
H2(g)+ 1/2 O2(g) ==== H2O (l) ΔH=-285.84kJ·mol-1
在 H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O (l)的热化学方程式为
。
(3)氢氟酸是一种弱酸,可用刻蚀玻璃。已知25 ℃时:
HF(aq)+OH-(aq)===F-(aq)+H2O(l) ΔH=-67.7 kJ·mol-1
H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1
则表示氢氟酸电离的热化学方程式为:
可见氢氟酸的电离是 的(填吸热或放热)。
查看答案和解析>>
科目:高中化学 来源: 题型:
U﹣235原子的裂变是目前人类利用核能的主要来源,下列有关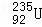 的说法正确的是( )
的说法正确的是( )
|
| A. |
| B. |
|
|
| C. |
| D. |
|
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | 金属氧化物一定是碱性氧化物 |
|
| B. | 只含有一种元素的物质一定是单质 |
|
| C. | 胶体与溶液的本质区别在于是否有丁达尔现象 |
|
| D. | 化学反应中元素的化合价都没变化的为非氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
现用质量分数为98%、密度为1.84g•cm﹣3的浓H2SO4来配制500mL0.2mol/L的稀H2SO4.
可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒⑥容量瓶 ⑦托盘天平 ⑧药匙.
请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时用到的有 (填代号).
(2)经计算,需浓H2SO4的体积为 5 .现有①10L ②50mL ③100mL三种规格的量筒,应选用的量筒是 (填代号).
(3)将浓H2SO4加适量蒸馏水稀释,冷却片刻,随后全部转移到 mL的容量瓶中,转移时应用玻璃棒 引流 .转移完毕,用少量蒸馏水洗涤 次,并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,振荡容量瓶,使溶液混合均匀.然后缓缓地把蒸馏水直接注入容量瓶直到液面接近刻度1﹣2cm处.改用 加蒸馏水到瓶颈刻度的地方,使溶液的凹面恰好与刻度相切.振荡、摇匀后,装瓶、贴签.
(4)在配制过程中,其他操作都准确,下列操作中:
能引起物质的量浓度偏低的是 ,能引起物质的量浓度偏高的有 (填代号).
①未等稀释后的硫酸冷却即转移到容量瓶中
②定容时,仰视刻度线
③转移前,容量瓶中含有少量蒸馏水.
查看答案和解析>>
科目:高中化学 来源: 题型:
铁镍蓄电池又称爱迪生电池,放电时的总反应为: Fe+Ni2O3+3H2O=Fe(OH)2+2Ni(OH)2
下列有关该电池的说法不正确的是 ( )
A.电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe
B.电池放电时,负极反应为Fe+2OH--2e-= Fe(OH)2
C.电池充电过程中,阴极附近溶液的pH降低
D.电池充电时,阳极反应为2Ni(OH)2+2OH--2e-=Ni2O3+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对化学平衡移动的分析中,不正确的是
①已达平衡的反应:C(s)+H2O(g) CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
②已达平衡的反应N2(g)+3H2(g) 2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
③有气体参加的反应平衡时,若减小反应器容积,平衡一定向气体体积增大的方向移动
④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动
A.①④ B.①②③ C.②③④ D.①②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com