

 .
.分析 A为含两种元素的化合物,B为无色气体单质,A、B在高温下反应生成C和D,C为能使品红溶液褪色的无色气体化合物,C应为SO2,D为红色固体氧化物,应为Fe2O3,所以B为O2,A为含有铁和硫元素的化合物,A中金属元素的质量分数为46.7%,所以A的化学式为FeS2,C与氧气反应生成E为SO3,J为常见的无色液体,应为H2O,E与水反应生成F为H2SO4,K、L为常见金属单质,G溶液为蓝色,所以K为Cu,铜与浓硫酸反应生成G为CuSO4,氧化铁与硫酸反应生成H为Fe2(SO4)3,H与铜反应生成I为FeSO4,铁与硫酸铜反应生成硫酸亚铁,所以L为Fe,据此答题.
解答 解:A为含两种元素的化合物,B为无色气体单质,A、B在高温下反应生成C和D,C为能使品红溶液褪色的无色气体化合物,C应为SO2,D为红色固体氧化物,应为Fe2O3,所以B为O2,A为含有铁和硫元素的化合物,A中金属元素的质量分数为46.7%,所以A的化学式为FeS2,C与氧气反应生成E为SO3,J为常见的无色液体,应为H2O,E与水反应生成F为H2SO4,K、L为常见金属单质,G溶液为蓝色,所以K为Cu,铜与浓硫酸反应生成G为CuSO4,氧化铁与硫酸反应生成H为Fe2(SO4)3,H与铜反应生成I为FeSO4,铁与硫酸铜反应生成硫酸亚铁,所以L为Fe,
(1)J为H2O,J的电子式为 ,
,
故答案为: ;
;
(2)根据上面的分析可知,A的化学式为FeS2,
故答案为:FeS2;
(3)铜 与浓硫酸在加热时反应的化学方程式为 Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(4)H为Fe2(SO4)3,K为Cu,H和K反应的离子方程式为2Fe3++Cu=2Fe2++Cu2+,
故答案为:2Fe3++Cu=2Fe2++Cu2+.
点评 本题考查无机物的推断,题目难度中等,注意根据相关物质的颜色以及转化关系作为该题的突破口,学习中注意相关知识的掌握.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
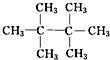
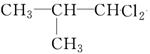 、
、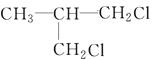 、
、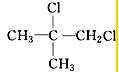 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 澄清的石灰水跟稀硝酸反应:Ca(OH)2+2H+=Ca2++2H2O | |
| B. | 氢氧化钡溶液和硫酸铜溶液反应:Ba2++SO42-=BaSO4↓ | |
| C. | 用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O | |
| D. | 往澄清石灰水中通入少量二氧化碳气体:CO2+OH-=HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{39m}{V}$mol•L-1 | B. | $\frac{2m}{39V}$mol•L-1 | C. | $\frac{m}{39V}$mol•L-1 | D. | $\frac{m}{78V}$mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
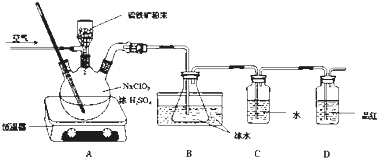
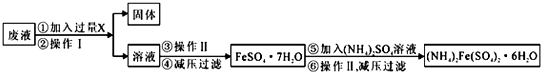
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 尿素[H2NCONH2]既是一种非常重要的高氮化肥,又是多种有机、无机产品的生产原料.工业上以合成氨厂的NH3和CO2为原料生产尿素.请回答下列问题:
尿素[H2NCONH2]既是一种非常重要的高氮化肥,又是多种有机、无机产品的生产原料.工业上以合成氨厂的NH3和CO2为原料生产尿素.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com