
| 100ρω |
| M |
| 1000×1.84×98% |
| 98 |
| 106g |
| m |
| 22.4L |
| 0.448L |
| 2.12g |
| 2.5g |


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
某同学用NaHCO3和KHCO3组成的混合物进行实验,测得如下数据(盐酸的物质的量浓度相等).下列分析推理不正确的是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
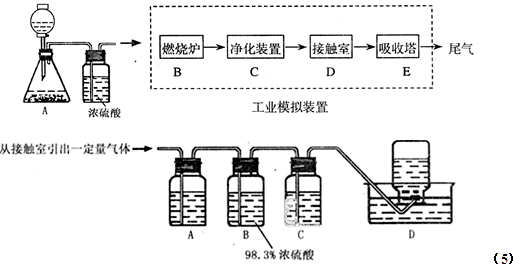
| ||
| ||
| ||
| ||
| 压强/Mpa 转化率 温度/℃ |
0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:

Ⅰ.已知A、B为单质,D为无机化合物,其余均为有机化合物;A、B在一定条件下可化合生成D;Z具有芳香气味;X、Y均为生活中常见有机物;X在催化剂作用下可与B反应生成C;相同条件下,C的蒸气密度是H2密度的22倍。C中碳元素的质量分数为54.5%,氢元素的质量分数为9.1%,其余为氧元素。请写出:
①反应X+Y![]() Z+D的化学方程式:_________________________________________;
Z+D的化学方程式:_________________________________________;
②A+C![]() X的反应类型:__________________________________________________;
X的反应类型:__________________________________________________;
③Y的一种同分异构体的结构简式:_______________________。
Ⅱ.已知A、B、C、D为单质,X、Y、Z为无机化合物。
(1)若B、D为同一种物质,请写出反应X+Y![]() Z+D的化学方程式(写出一个即可):_______________________________________________。
Z+D的化学方程式(写出一个即可):_______________________________________________。
(2)若C、D为同一种物质:
①化合物Z中所含的元素为______________(用A、B、C表示)。
②反应X+Y![]() Z+D是否为氧化还原反应?请说明理由。
Z+D是否为氧化还原反应?请说明理由。
③某同学认为:C元素在化合物X、Y中呈现的化合价,必定是在一种物质中呈正价,在另一种物质中呈负价。请你判断该结论是否正确,并用有关的化学方程式证明你的结论。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质A、B、C、D、X、Y、Z之间转化关系如下图所示:

I.已知A、B为单质,D为无机化合物,其余均为有机化合物;A、B在一定条件下可化合生成D;Z具有芳香气味;X、Y均为生活中常见有机物;X在催化剂作用下可与B反应生成C;相同条件下,C的蒸气密度是H2密度的22倍。C中碳元素的质量分数为54.5%,氢元素的质量分数为9.1%,其余为氧元素。请写出:
①反应X+Y→Z+D的化学方程式:______________________
②A+C→X的反应类型:_______________________
③Y的一种同分异构体的结构简式:_______________________
Ⅱ.已知A、B、C、D为单质,X、Y、Z为无机化合物。
(1)若B、D为同一种物质,请写出反应X+Y→Z+D的化学方程式(写出一个即可):
___________________________________________
(2)若C、D为同一种物质:
①化合物Z中所含的元素为_________(用A、B、C表示)。
②反应X+Y→Z+D是否为氧化还原反应?请说明理由。
③某同学认为:C元素在化合物X、Y中呈现的化合价,必定是在一种物质中呈正价,在另一种物质中呈负价。请你判断该结论是否正确,并用有关的化学方程式证明你的结论。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com