
分析 (1)碘遇淀粉溶液变蓝色,当完全反应时,溶液褪色;
(2)硫代硫酸钠溶液显碱性,应选择碱式滴定管;
(3)溶液呈蓝色,随反应I2+2Na2S2O3=2NaI+2Na2S4O6进行,溶液中没有碘,溶液由蓝色为无色;
(4)根据反应Cl2+2I-=2Cl-+I2,I2+2Na2S2O3=2NaI+Na2S4O6结合c=$\frac{n}{V}$进行计算;
(5)步骤②碱式滴定管未用Na2S2O3溶液润洗,使得Na2S2O3溶液浓度偏小判断.
解答 解:(1)溶液中有单质碘,加入淀粉溶液呈蓝色,碘与亚硫酸钠发生氧化还原反应,当反应终点时,蓝色褪去;
故答案为:淀粉溶液;
(2)硫代硫酸钠溶液显碱性,应选择碱式滴定管;
故答案为:碱;
(3)碘遇淀粉变蓝色,所以溶液呈蓝色,随反应I2+2Na2S2O3=2NaI+2Na2S4O6进行,溶液中没有碘,溶液由蓝色为无色,说明反应到终点,判断达到滴定终点的实验现象是:滴最后一滴溶液,由蓝色恰好变为无色,且半分钟内不变色;
故答案为:滴最后一滴溶液,由蓝色恰好变为无色,且半分钟内不变色;
(4)根据反应Cl2+2I-=2Cl-+I2,I2+2Na2S2O3=2NaI+Na2S4O6;
则有Cl2~2Na2S2O3
1 2
n 0.01mol•L-1×0.0200L
n=0.0001ml
c(Cl2)=$\frac{0.0001mol}{0.0100L}$=0.01mol/L;
故答案为:0.01mol/L;
(5)碱式滴定管未用Na2S2O3溶液润洗,使得Na2S2O3溶液浓度偏小,消耗的Na2S2O3溶液体积偏大,测得I2的物质的量偏多,所以实验中的一处明显错误为步骤②滴定管用蒸馏水洗净后未用待测液润洗,故答案为:步骤②滴定管用蒸馏水洗净后未用待测液润洗.
点评 本题考查了氧化还原滴定的相关操作和计算,注意掌握氧化还原滴定的原理和方法是解题的关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 通入大量O2 | B. | 增大容器容积 | C. | 移去部分SO3 | D. | 降低体系温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 碱性氧化物 氧化铁 Fe2O3 | B. | 酸性氧化物 干冰 CO2 | ||
| C. | 酸 硫酸 H2S | D. | 碱 纯碱 Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作 | 测定结果评价 |
| A | 酸式滴定管在装液前未用标准盐酸润洗2~3次 | 偏高 |
| B | 开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失 | 偏高 |
| C | 锥形瓶未干燥 | 无影响 |
| D | 盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次 | 偏低 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
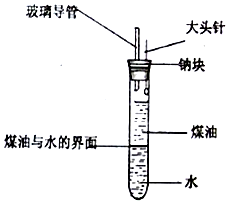 某化学研究性学习小组设计了如图所示的实验装置,目的是做钠与水反应的实脸并验证①钠的物理性质;②钠和水反应的产物.请回答下列问题:
某化学研究性学习小组设计了如图所示的实验装置,目的是做钠与水反应的实脸并验证①钠的物理性质;②钠和水反应的产物.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150ml | B. | 180ml | C. | 200ml | D. | 250ml |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
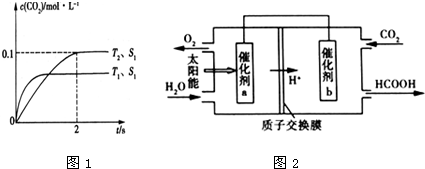
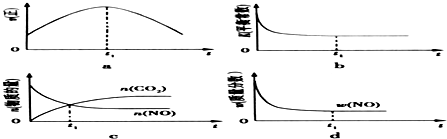
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com