
| A、取a克混合物充分加热,减重b克 |
| B、取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克 |
| C、取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体 |
| D、取a 克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得 b 克固体 |


科目:高中化学 来源: 题型:
| A、酸雨是指pH<5.6的雨水 |
| B、我国主要以硫酸型酸雨为主 |
| C、酸雨降到地面上后,酸性会逐渐增强 |
| D、空气中CO2和SO2的含量过高是形成酸雨的主要原因 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol 硫酸钾中阴离子所带电荷数为NA |
| B、乙烯和环丙烷(C3H6)组成的28g混合气体中含有NA个氢原子 |
| C、标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为NA |
| D、将0.1mol氯化铁溶于1L水中,所得溶液含有0.1NA Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 | ||||||||||
| B、向Cr2O72-+H2O?2CrO42-+2H+的平衡体系中滴加10~20滴6mol/LNaOH溶液颜色由橙色变黄色 | ||||||||||
C、500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为 N2(g)+3H2(g)
| ||||||||||
D、已知:
 的△H为-384 kJ?mol-1 的△H为-384 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲酸乙酯(HCOOC2H5) |
| B、乙酸乙酯(CH3COOC2H5) |
| C、葡萄糖(C6H12O6) |
| D、淀粉〔(C6H10O5)n〕 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| NaCN |
| HCl |
| 水解 |
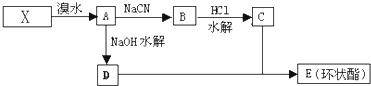
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
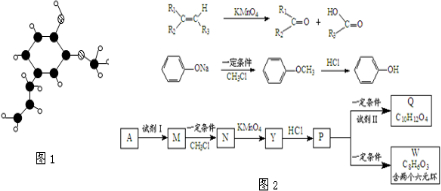
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com