
| A、甲酸乙酯(HCOOC2H5) |
| B、乙酸乙酯(CH3COOC2H5) |
| C、葡萄糖(C6H12O6) |
| D、淀粉〔(C6H10O5)n〕 |


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
| A、化学面对现代日益严重的环境问题显得越来越无能为力了 |
| B、化学是“污染”的代名词,一切污染皆因化学而起 |
| C、化学及分支学科面临着罕见的窘境,被人们淡忘、不重视是合乎情理的 |
| D、能源和环境问题的解决,过去、现在和将来都有赖于化学学科的发展 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用氯化铁溶液腐蚀铜板:Fe3++Cu=Fe2++Cu2+ |
| B、将少量的二氧化硫气体通入次氯酸钠溶液中 SO2+H2O+2ClO-=SO32-+2HClO |
| C、用氢氧化钡溶液中和硫酸氢铵溶液:H++SO42-+Ba2++OH-=H2O+BaSO4↓ |
| D、用纯碱溶液溶解苯酚:CO32-+C6H5OH→HCO3-+C6H5O- |
查看答案和解析>>
科目:高中化学 来源: 题型:
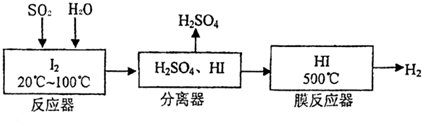

| 改进的操作或装置(注明必要的试剂) | 改进的作用 |
| 使用分液漏斗滴加浓硫酸 | 控制反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
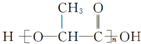 ,有关W的信息如图,据此回答下列问题:
,有关W的信息如图,据此回答下列问题: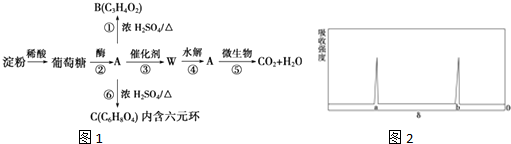
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、取a克混合物充分加热,减重b克 |
| B、取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克 |
| C、取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体 |
| D、取a 克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得 b 克固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在卤代烃中直接加入AgNO3溶液 |
| B、加蒸馏水,充分搅拌后,加入AgNO3溶液 |
| C、加入NaOH溶液,加热后加入稀硝酸酸化,再加入AgNO3溶液 |
| D、加入NaOH的乙醇溶液,加热后加入AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 温度/℃ | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
| 溶解度 (g/100g H2O) | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
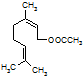 乙酸橙花酯是一种食用香料,结构如图所示.下列关于该物质的说法有:
乙酸橙花酯是一种食用香料,结构如图所示.下列关于该物质的说法有:| A、①③④ | B、②③⑤ |
| C、①④⑤ | D、①③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com