
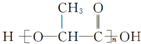 ,有关W的信息如图,据此回答下列问题:
,有关W的信息如图,据此回答下列问题: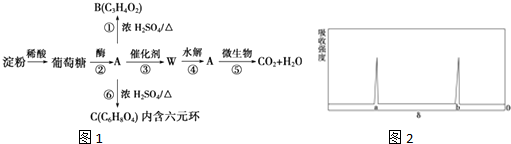
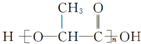 ,则A为
,则A为 ,A发生缩聚反应生成W,由B的分子式可知,A分子内脱去1分子水生成B,B应为CH2=CHCOOH,2分子A发生酯化反应生成环酯C为
,A发生缩聚反应生成W,由B的分子式可知,A分子内脱去1分子水生成B,B应为CH2=CHCOOH,2分子A发生酯化反应生成环酯C为 ,(4)中B分子有多种同分异构体,其中X的核磁共振氢谱有个吸收峰,且峰面积之比为1:1,含有2种H原子,且氢原子数目相等,X的结构简式可能为OHCCH2CHO、
,(4)中B分子有多种同分异构体,其中X的核磁共振氢谱有个吸收峰,且峰面积之比为1:1,含有2种H原子,且氢原子数目相等,X的结构简式可能为OHCCH2CHO、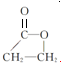 、
、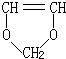 ,据此解答.
,据此解答.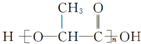 ,则A为
,则A为 ,A发生缩聚反应生成W,由B的分子式可知,A分子内脱去1分子水生成B,B应为CH2=CHCOOH,2分子A发生酯化反应生成环酯C为
,A发生缩聚反应生成W,由B的分子式可知,A分子内脱去1分子水生成B,B应为CH2=CHCOOH,2分子A发生酯化反应生成环酯C为 ,
, 发生消去反应生成CH2=CHCOOH,故答案为:消去反应;
发生消去反应生成CH2=CHCOOH,故答案为:消去反应;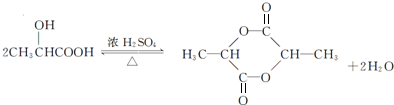 ,
, ;
; 、
、 ,可以用新制银氨溶液(或新制氢氧化铜悬浊液)、Br2的CCl4溶液鉴别X,
,可以用新制银氨溶液(或新制氢氧化铜悬浊液)、Br2的CCl4溶液鉴别X, 、
、 ;新制银氨溶液(或新制氢氧化铜悬浊液)、Br2的CCl4溶液;
;新制银氨溶液(或新制氢氧化铜悬浊液)、Br2的CCl4溶液;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
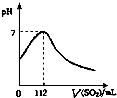 在标准状况下,向100mL氢硫酸溶液中通入二氧化硫气体,溶液pH变化如图所示,则原氢硫酸溶液的物质的量浓度为( )
在标准状况下,向100mL氢硫酸溶液中通入二氧化硫气体,溶液pH变化如图所示,则原氢硫酸溶液的物质的量浓度为( )| A、0.5 mol?L─1 |
| B、0.05 mol?L─1 |
| C、1 mol?L─1 |
| D、0.1 mol?L─1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯化铝溶液中加入过量氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| B、AlCl3 溶液中投入过量Na:Al3++4Na+2H2O=AlO2-+4Na++2H2↑ |
| C、苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
| D、碳酸氢铵溶液中加入过量氢氧化钠溶液:HCO3-+OH-=CO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | 颜色和状态 | 密度/g?cm3 | 0℃时溶解度/g | 100℃时溶解度/g |
| KCl | 无色晶体 | 1.98 | 27.6 | 56.7 |
| KClO3 | 无色晶体 | 2.32 | 3.3 | 57 |
| KClO4 | 无色晶体 | 2.32 | 0.75 | 21.8 |
| 1 |
| 3 |
| 1 |
| 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲酸乙酯(HCOOC2H5) |
| B、乙酸乙酯(CH3COOC2H5) |
| C、葡萄糖(C6H12O6) |
| D、淀粉〔(C6H10O5)n〕 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| O | - 4 |
| 实验 编号 | 反应温度 (利用水浴加热) | 稀硫酸溶液 | MnSO4固体 | 0.10mol/LKMnO4溶液 | 褪色时间 |
| 1 | 65℃ | - | - | 1.0mL | 100s |
| 2 | 65℃ | 10滴 | - | 1.0mL | 90s |
| 3 | 75℃ | 10滴 | - | 1.0mL | 40s |
| 4 | 75℃ | 10滴 | 加入少许 | 1.0mL | 3s |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | ② | ③ | ④ | ⑤ | ⑥ | |
| 原子半径(10-10m) | 1.30 | 0.82 | 0.99 | 1.11 | 0.90 | 1.18 |
| 最高或最低化合价 | +2 | +3 | +7 | +4 | +2 | +3 |
| -1 | -4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com