
【题目】Na2CO3、NaCl、 NaOH、Na2SO4可按不同标准分类,下列分类标准不正确的是
A. 钠的化合物 B. 纯净物 C. 钠盐 D. 无机物
科目:高中化学 来源: 题型:
【题目】对于反应4Fe(OH)2(s)+O2(g)+2H2O(l)=4Fe(OH)3(s) △H= - 444.3kJ/mol,在常温常压下能自发进行,对反应的方向起决定性作用的是
A. 焓变 B. 温度 C. 压强 D. 熵变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某一恒温体积可变的密闭容器中发生如下反应:A(g)+B(g)![]() 2C(g) ΔH<0,某时刻达到平衡后,在
2C(g) ΔH<0,某时刻达到平衡后,在![]() 时刻改变某一条件,其反应过程如图所示。下列说法正确的是( )
时刻改变某一条件,其反应过程如图所示。下列说法正确的是( )

A. ![]()
B. I、Ⅱ两过程达到平衡时,A的体积分数I>II
C. ![]() 时刻改变的条件是向密闭容器中加C
时刻改变的条件是向密闭容器中加C
D. I、II两过程达到平衡时,平衡常数I<II
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将浓度均为0.1mol/L,体积分别为Va和Vb的HA溶液与BOH溶液按不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液pH的关系如图所示,下列说法正确的是( )

A. Ka(HA)=1×10-6mol/L
B. b点c (B+)=c(A-)=c(OH-)=c(H+)
C. c点时,![]() 随温度升高而减小
随温度升高而减小
D. a→c过程中水的电离程度始终增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于蛋白质的下列叙述中,错误的是( )
A. 蛋白质水溶液具有胶体的性质 B. 所有的蛋白质都能人工合成
C. 蛋白质水解的最终产物是氨基酸 D. 蛋白质分子中既含有氨基又含有羧基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关仪器的使用或实验操作正确的是( )
A. 蒸发NaCl溶液获取NaCl晶体,要将溶液中的水分蒸干
B. 使用容量瓶配制一定物质的量浓度溶液时,要先检验容量瓶是否漏水
C. 用托盘天平称量6.25克Na2CO3
D. 可以使用酒精萃取碘水中的碘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知醋酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+ K=1.75×10-5。
CH3COO-+H+ K=1.75×10-5。
(1)计算0.01mol/L的CH3COOH溶液的pH=_________。(已知lg1.75=0.24)
(2)25℃,将0.1mol/L的CH3COOH溶液和0.1mol/L的NaOH溶液等体积混合后溶液的pH=10,则该混合溶液中由水电离出的c(OH-)=___________mol/L,写出该混合溶液中下列算式的精确结果(不能做近似计算),c(Na+)-c(CH3COO-)=______________mol/L。
(3)下列方法中,可以使0.10 mol·L-1 CH3COOH的电离程度增大的是___________
a.加入少量0.10 mol·L-1的稀盐酸 b.加热CH3COOH溶液
c.加水稀释至0.010 mol·L-1 d.加入少量冰醋酸
e.加入少量镁粉 f.加入少量0.10 mol·L-1的NaOH溶液
(4)SOCl2是一种液态化合物,向盛有10mL水的锥形瓶中,小心滴加8~10滴SOCl2,可观察到剧烈反应,液面上有雾形成,产生可以使品红溶液褪色的气体,往溶液中滴加AgNO3溶液,有白色沉淀析出,请写出SOCl2与水反应的化学方程式______________________________,蒸干AlCl3溶液不能得到无水AlCl3,用SOCl2和AlCl3·6H2O混合加热可以得到无水AlCl3,试解释原因______________________
(5)常温下,反应NH4++HCO3-+H2O ![]() NH3·H2O+H2CO3的平衡常数K=__________。(已知常温下,NH3·H2O的电离平衡常数Kb = 2×10-5,H2CO3的电离平衡常数Ka1 = 4×10-7,Ka2 = 4×10-11)
NH3·H2O+H2CO3的平衡常数K=__________。(已知常温下,NH3·H2O的电离平衡常数Kb = 2×10-5,H2CO3的电离平衡常数Ka1 = 4×10-7,Ka2 = 4×10-11)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有短周期主族元素X,Y,Z,R,T,R原子的最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Y与T同主族.五种元素原子半径与原子序数之间的关系如图所示.下列推断正确的是( ) 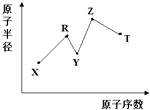
A.离子半径:Y<Z
B.氢化物的沸点:Y<T
C.最高价氧化物对应水化物的酸性:T<R
D.由X,Y,Z,R四种元素组成的常见化合物中含有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质所含化学键类型和化合物类型判断完全正确的一组是 ( )
A. Na2O2 离子键 离子化合物 B. MgCl2 离子键、共价键 离子化合物
C. F2 共价键 共价化合物 D. NaOH 离子键、共价键 离子化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com