
【题目】N2和H2合成NH3的能量变化如图所示,该反应的热化学方程式是( )

A. N2(g)+3H2(g) = 2NH3(g) ;△H = 2(b—a) kJ/mol
B. N2(g)+3H2(g) = 2NH3(l);△H = 2(a—b—c) kJ/mol
C. ![]() N2(g)+
N2(g)+![]() H2(g) = NH3(l) ;△H = (b+c—a) kJ/mol
H2(g) = NH3(l) ;△H = (b+c—a) kJ/mol
D. ![]() N2(g)+
N2(g)+![]() H2(g) =NH3(g) ;△H = (a+b) kJ/mol
H2(g) =NH3(g) ;△H = (a+b) kJ/mol
科目:高中化学 来源: 题型:
【题目】化合物Z由如下反应得到:C4H9Br![]() Y
Y![]() Z,Z的结构简式不可能是( )
Z,Z的结构简式不可能是( )
A.CH3CH2CHBrCH2Br
B.CH3CH(CH2Br)2
C.CH3CHBrCHBrCH3
D.CH2BrCBr(CH3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】V mLAl2(SO4)3溶液中含有Al3+ a g,取![]() V mL溶液稀释到4V mL,则稀释后溶液中S042-的物质的量浓度是
V mL溶液稀释到4V mL,则稀释后溶液中S042-的物质的量浓度是
A. ![]() mol/L B.
mol/L B. ![]() mol/L
mol/L
C. ![]() mol/L D.
mol/L D. ![]() mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关热化学方程式书写与对应表述均正确的是
A. 稀硫酸与0.1 mol/L NaOH溶液反应:H+(aq)+OH-(aq)= H2O(l) △H = +57.3 kJ·mol1
B. 已知2C(s)+O2(g)=2CO(g) △H=—221 kJ·mol-1, 则可知C的燃烧热为110.5 kJ·mol1
C. 密闭容器中,0.3mol硫粉与0.2mol铁粉混合加热生成硫化亚铁0.2mol时,放出19.12 kJ热量。则Fe(s)+S(s)=FeS(s) △H= - 95.6 kJ·mol1
D. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) + 3H2(g) ![]() 2NH3(g) △H= —38.6kJ·mol1
2NH3(g) △H= —38.6kJ·mol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取1.06g Na2CO3溶于水配成100ml溶液,求:
(1)Na2CO3溶液的物质的量浓度;________________
(2)Na+ 物质的量浓度; ______________
(3)取出20.0ml该溶液用蒸馏水稀释,使Na2CO3溶液物质的量浓度变为0.04mol/L,求稀释后溶液的体积。_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】许多物质与身体健康有着密切关系,请结合所学知识,判断下列叙述中错误的是( )
A. 缺镁易患心血管病,缺碘易患甲状腺肿大
B. 在医疗上FeCl3常用作止血剂,ZnSO4常用作收敛剂
C. 葡萄糖、食盐、味精均可作食品添加剂
D. 苏丹红是一种呈红色的有机物,能当作辣椒红色素用于食品加工
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,乙装置中充入滴有酚酞的氯化钠溶液,X、Y均为石墨电极。反应一段时间后,乙装置X极附近溶液先变红。下列判断中正确的是
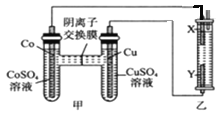
A. 电子流向:Cu电极→Y→X→Co电极
B. 钴(Co)的金属性比铜的强
C. 工作时,SO42-向Cu电极移动
D. 转移0.2mol e-,乙中生成0.2molNaClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁铜是人类最早大规模使用的金属,它们的化合物在科学研究和工业生产中具有许多用途。请回答以下问题:
(1)铁元素在周期表中的位置是____,铜的基态原子核外电子排布式为______ 。
(2)二茂铁[Fe(C5H5)2],橙色晶型固体,有类似樟脑的气味,抗磁性。熔点172.5~173℃,100℃以上升华,沸点249℃。据此判断二茂铁晶体类型为______________。
(3)蓝矾(CuSO4·5H2O)的结构如下图所示:

图中虚线表示_____________,SO42-的立体构型是__________,NO3-中N原子的杂化轨道类型是___________;O原子的价电子排布图为__________________。
(4)铁有δ、γ、α三种同素异形体,下图是它们的晶体结构图,三种晶体中铁原子周围距离最近的铁原子个数之比为______。

(5)某种具有储氢功能的铜合金晶体具有立方最密堆积的结构,晶胞中Cu原子处于面心,Au原子处于顶点位置,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与 CaF2的结构(晶胞结构如图)相似,该晶体储氢后的化学式为________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com