
 A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,如图是它们之间的相互转化关系.请回答:
A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,如图是它们之间的相互转化关系.请回答:
| ||


科目:高中化学 来源: 题型:
 |
 |
 |
 |
| ① | ② | ③ | ④ |
| A、实验①烧杯中的澄清石灰水都变浑浊 |
| B、实验②试管中出现砖红色沉淀 |
| C、实验③品红溶液褪色 |
| D、实验④气体由红棕色变为无色,试管中的液面上升 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
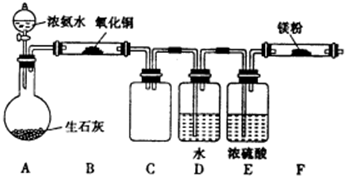
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选用试剂(填代号) | 实验现象 | |
| 第一种方法 | ||
| 第二种方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| 步骤 | 实验操作 | 实验现象、结论 |
| 1 | 取一定量3mol/L硫酸溶液于试管中,加热煮沸去除溶解氯气 | / |
| 2 | 取少量产品于试管中,加适量步骤1处理好的溶液,溶解、配成溶液 | 固体溶解,溶液呈浅黄色 |
| 3 | 取少量步骤2配好的溶液于试管中,滴加几滴20%硫氰化钾溶液,振荡 | |
| 4 | |
| 1 |
| 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 碳、氮、氧、铜是与人类生产三生活息息相关的化学元素,请回答下列问题:
碳、氮、氧、铜是与人类生产三生活息息相关的化学元素,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| 主要成分 | NaHCO3 | Mg(OH)2 |
| 主要成分相对分子质量 | 84 | 58 |
| 建议每次剂量/g | 0.5 | 0.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
48 22 |
| A、质子数为48 |
| B、原子序数为22 |
| C、质量数为22 |
| D、中子数为48 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com