
A、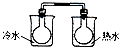 NO2球浸在冷水和热水中 | ||||||||
B、
| ||||||||
C、 | ||||||||
D、
|


科目:高中化学 来源: 题型:
| A、1mol钠与O2反应生成Na2O 或Na2O2,转移的电子数目均为2NA |
| B、1molO2和足量的Mg或Al完全反应,电子转移数目之比为2:3 |
| C、Na、Mg、Al各1mol和足量的O2反应,电子转移数目之比为1:2:3 |
| D、Cu、Mg各1mol在O2中充分燃烧,电子转移数目之比为3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(NO)=0.001 mol/(L?s) |
| B、v(H2O)=0.001 mol/(L?s) |
| C、v(NH3)=0.002 mol/(L?s) |
| D、v(O2)=0.015mol/(L?s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHCO3═Na++H++CO32- |
| B、KClO3═K++Cl-+3O2- |
| C、NaHSO4═Na++H++SO42- |
| D、NH3?H2O═NH4++OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )| A、原子半径:W>Z>Y>X |
| B、含Y元素的盐溶液一定显酸性 |
| C、最简单气态氢化物的热稳定性:Z>W |
| D、X与氢元素组成的化合物XH5与水反应可产生两种气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com