
【题目】市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料。这种电池的电池反应式为:Li+2Li0.35NiO2![]() 2Li0.85NiO2,下列说法不正确的是( )
2Li0.85NiO2,下列说法不正确的是( )
A.放电时,负极的电极反应式:Li-e-=Li+
B.充电时,Li0.85NiO2既发生氧化反应又发生还原反应
C.该电池不能用水溶液作为电解质溶液
D.放电过程中Li+向负极移动
科目:高中化学 来源: 题型:
【题目】周期表前四周期的元素a、b、c、d、e,原子序数依次增大.a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子.回答下列问题:
(1)b、c、d中第一电离能最大的是______![]() 填元素符号
填元素符号![]() ,
,
(2)a和其他元素形成的二元共价化合物中,分子中既含有极性共价键、又含有非极性共价键的化合物是______![]() 填化学式,写出两种
填化学式,写出两种![]() .
.
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是______;酸根呈三角锥结构的酸是______![]() 填化学式
填化学式![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素 R、T、Q、W 在元素周期表中的相对位置如图所示,其中 T 所处的周期序数与族序数相等下列判断不正确的是

A.最简单气态氢化物的热稳定性:R >Q
B.最高价氧化物对应水化物的酸性:Q< W
C.R 的氧化物是酸性氧化物
D.含 T 的盐溶液可能显酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】冬季是雾霾天气高发的季节,其中汽车尾气和燃煤尾气是造成雾霾的原因之一。
(1)使用甲醇汽油可以减少汽车尾气对环境的污染。工业上在 200℃和 10MPa 的条件下可用甲烷和氧气通过铜制管道反应制得甲醇,已知一定条件下,CH4 和 CH3OH 的燃烧热分别 784kJ/mol 和 628kJ/mol 则 2CH4(g)+O2(g)![]() 2CH3OH(g) △H=_____。
2CH3OH(g) △H=_____。
(2)二甲醚也是清洁能源。用合成气在催化剂存在下制备二甲醚的反应原理为:2CO(g)+4H2(g) CH3OCH3(g) +H2O(g) △H<0。某温度下,,将 2.0molCO(g)和 6.0molH2(g)充入容积为 2L 的密闭容器中,反应到达平衡时, 改变压强和温度,平衡体系中 CH3OCH3(g)的物质的量分数变化情况如图所示,关于温度和压强的关系判断正确的是_____。
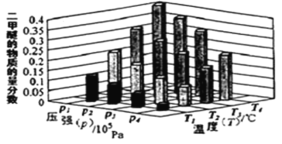
A.p3>p2,T3>T2
B.p1>p3,T1>T3
C.p1>p4,T2>T3
D.p2>p4,T4>T2
(3)汽车尾气净化的主要原理为:2NO(g)+2CO(g)![]() 2CO2(g) +N2(g);
2CO2(g) +N2(g);
①200K、pPa时,在一个容积为 2L的恒温密闭容器中充入 1.5molNO 和 2.0molCO,开始反应至 2min 时测得 CO 转化率为 30%,则用N2表示的平均反应速率为v(N2)=_________;反应达到平衡状态时,测得二氧化碳为 0.8mol,则平衡时的压强为起始压强的_________倍(保留两位小数)。
②该反应在低温下能自发进行,该反应的ΔH_____0(填“>”、“<”)
(4)一定温度下,将NO2与SO2以体积比 1:2 置于密闭容器中发生反应NO2(g)+SO2(g) SO3(g)+NO(g),达到平衡时SO3的体积分数为 25%。该反应的平衡常数K= ______。
(5)利用原电池反应可实现NO2 的无害化,总反应为6NO2+ 8NH3=7N2+12H2O,电解质溶液为碱性。工作一段时间后,该电池正极区附近溶液 pH ____(填“变大”、“变小”或“不变”),负极电极反应式为 ____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硅是一种高温陶瓷材料,它硬度大、熔点高,化学性质稳定,工业上普遍采用高纯硅与纯氮在1 300 ℃反应获得。
(1)根据性质,推测氮化硅陶瓷的用途是________。(填序号)
A.制汽轮机 | B.制有色玻璃 |
C.制永久性模具 | D.制造柴油机 |
(2)写出N的原子结构示意图__________,根据元素周期律知识,请写出氮化硅的化学式_________________。
(3)氮化硅陶瓷抗腐蚀能力强,除氢氟酸外,它不与其他无机酸反应,试推测该陶瓷被氢氟酸腐蚀的化学方程式___________________________________。
(4)现用四氯化硅与氮气在氢气气氛保护下,加强热发生反应,可得较高纯度的氮化硅,反应的化学方程式为_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以二氧化锰为原料制取高锰酸钾晶体的实验流程如图所示,下列有关说法正确的是
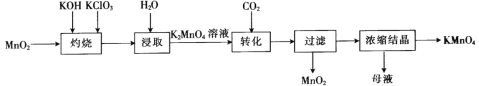
A.“灼烧”时,可在玻璃坩埚中进行
B.“浸取”时,可用无水乙醇代替水
C.“转化”反应中,通入CO2的目的是提供还原剂
D.“浓缩结晶”的目的是分离提纯KMnO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对氨基苯甲酸(![]() )是一种用途广泛的化工产品和医药中间体,以对硝基苯甲酸(
)是一种用途广泛的化工产品和医药中间体,以对硝基苯甲酸(![]() )为原料,采用电解法合成对氨基苯甲酸的装置如图。下列说法正确的是
)为原料,采用电解法合成对氨基苯甲酸的装置如图。下列说法正确的是

A.电子由金属阳极DSA经导线流入直流电源
B.阴极的主要电极反应式为![]() +6e-+6H+→
+6e-+6H+→![]() +2H2O
+2H2O
C.每转移1mole-时,阳极电解质溶液的质量减少8g
D.反应结束后阳极区pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾由多种污染物形成,包含颗粒物(PM2.5)、氮氧化物(NOx)、CO、SO2等。化学在解决雾霾污染问题中有着重要的作用。
(1)已知:①2CO(g)+O2(g)=2CO2(g)△H1=-566.0kJ·mol-1
②N2(g)+2O2(g)=2NO2(g)△H2=+64kJ·mol-1
反应2NO2(g)+4CO(g=N2(g)+4CO2(g)在__________(填“高温”或“低温”)条件下能自发进行。
(2)研究发现利用NH3可除去硝酸工业尾气中的NO。NH3与NO的物质的量之比分别为1:2、1:1.5、3:1时,NO脱除率随温度变化的曲线如图1所示。

①曲线a中,NO的起始浓度为6×10-4mg·m-3,若从X点到Y点经过20s,则该时间段内NO的脱除速率为_________mg·m-3·s-1。
②曲线c对应的NH3与NO的物质的量之比是________,其理由是__________
(3)炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化氧可以快速氧化SO2。活化过程中的能量变化模拟计算结果如图2所示。无水情况下,一个氧分子的活化能为__________,容易活化氧分子的条件是_________(填“有水”或“无水”)。
(4)若反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g)的正、逆反应速率分别可表示为v正=k正c2(NO)·c2(CO);v逆=k逆c(N2)·c2(CO2),k正、k逆分别为正、逆反应速率常数,c为物质的量浓度。一定温度下,在体积为1L的恒容密闭容器中加入4molNO和4molCO发生上述反应,测得CO和CO2的物质的量浓度随时间的变化如图3所示。
N2(g)+2CO2(g)的正、逆反应速率分别可表示为v正=k正c2(NO)·c2(CO);v逆=k逆c(N2)·c2(CO2),k正、k逆分别为正、逆反应速率常数,c为物质的量浓度。一定温度下,在体积为1L的恒容密闭容器中加入4molNO和4molCO发生上述反应,测得CO和CO2的物质的量浓度随时间的变化如图3所示。

①a点时,v逆:v正=_____________。
②测得平衡时体系压强为p,KP为用气体分压表示的平衡常数,分压=总压×物质的量分数,则平衡常数KP=____________(用含p的式子表示)。
(5)某研究小组探究该反应中催化剂对脱氮率(NO的转化率)的影响。将等物质的量的NO和CO以一定的流速分别通过催化剂a、b,发生反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g)。相同时间、不同温度下测得使用催化剂a时脱氮率与温度的关系如图4中曲线Ⅰ所示。已知催化效率b>a,催化剂b的活性在450℃时最大(未达平衡)。请在图4中画出使用催化剂b时所对应的曲线(从300℃开始画)。_______________
N2(g)+2CO2(g)。相同时间、不同温度下测得使用催化剂a时脱氮率与温度的关系如图4中曲线Ⅰ所示。已知催化效率b>a,催化剂b的活性在450℃时最大(未达平衡)。请在图4中画出使用催化剂b时所对应的曲线(从300℃开始画)。_______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com