
����Ŀ����������װ������֤CaSO4��̿�����ȷ���������ԭ��Ӧ���һ�ԭ������SO2�������й�˵������ȷ����
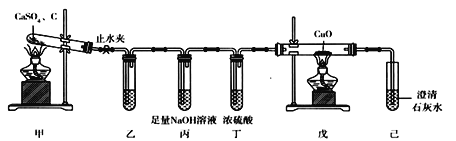
A. װ��������֤�����еĻ�ԭ���������ʢ��CaSO4��Һ
B. װ�ñ���װ�ö��������dz�ȥSO2��������������
C. װ�����к�ɫ��ĩ��죬���г��ְ�ɫ������˵������������CO
D. ʵ�����ʱ��Ӧ���ȹر�ֹˮ�У���Ѹ��Ϩ��װ�ü��еľƾ���
���𰸡�A
��������CaSO4��̿�����ȷ���������ԭ��Ӧ���һ�ԭ������SO2����ԭ�ӻ��ϼ۽��ͣ���̼Ԫ�ػ��ϼ����ߣ�����������Ϊ������̼��һ����̼��A. װ��������֤�����еĻ�ԭ����SO2����Ҫ������ʢ��Ʒ����Һ����A����B. Ҫ��֤���ɵ����������Ҫ��ȥ���������ˮ������װ�ñ���װ�ö��������dz�ȥSO2��ˮ��������B��ȷ��C. װ�����к�ɫ��ĩ��죬˵������������ͭ�Ļ�ԭ��Ӧ���������г��ְ�ɫ������˵������������CO��������ͭ����Ϊ������̼����C��ȷ��D. Ϊ�˷�ֹ������ʵ�����ʱ��Ӧ���ȹر�ֹˮ�У���Ѹ��Ϩ��װ�ü��еľƾ��ƣ���D��ȷ����ѡA��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��C��D��Ϊ������Ԫ�أ����ǵ�ԭ���������ε����� A�������Ϊһ�����ӵķǽ���Ԫ�أ�C ԭ�ӵ������������Ǵ�����3���� C��D���γ����ֹ�̬���������һ��Ϊ����ɫ���壻B��C���γɶ�����̬�����A��B��C����Ԫ�ؿ����γ����Ӿ��壬�þ����и�Ԫ��ԭ�ӵ����ʵ���֮��ΪA:B:C=4:2:3��
��ش��������⣺
��1��д��B��ԭ�ӽṹʾ��ͼ______��д��C��D�γɵĵ���ɫ���廯����ĵ���ʽ_____��
��2��Ԫ��ԭ�ӵ����ʵ���֮��ΪA:B:C=4:2:3�ľ�������Ϊ__________��
��3����д����A2C��BA3�����е�������ͬ��������A��B��CԪ������������Ԫ����ɵ����ķ��ţ���������____��_____��
��4��д����B��CԪ�������Ԫ��ԭ��������ΪB:C=7:12�Ļ�����Ļ�ѧʽ _______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��300mL0.5mol/L��FeCl3��Һ��0.2L1.0mol/L��KCl��Һ��Cl����Ũ��֮��Ϊ
A. 1��2B. 3��2C. 3��4D. 9��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����н�������A��B��C������ס����Լ�����D��E��F��G��H������֮����ת����ϵ��ͼ��ʾ(ͼ����Щ��Ӧ��������ͷ�Ӧ������û�б��)��

��ش��������⣺
��1��д���������ʵĻ�ѧʽ��B________����________��
��2��д�����з�Ӧ�����ӷ���ʽ��
��Ӧ��____________________________________��
��Ӧ��____________________________________��
��Ӧ��____________________________________��
��3����0.4 g D��1.06 g Na2CO3��ϲ������Һ��������Һ����εμ�0.1 mol��L��1ϡ���ᡣ������ͼ��ʾ������ϵ�л�������ȷ��ʾ������������������CO2�����ʵ����Ĺ�ϵͼ��________________

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȷ���� �� )
A. F2��Cl2��Br2��I2������������ǿ
B. VIA��Ԫ�ص�ԭ�ӣ���뾶Խ��Խ���õ�����
C. ͬ����Ԫ���У�VIIA��Ԫ�ص�ԭ�Ӱ뾶���
D. Ԫ�����ڱ��д�IIIB��IIB��10�����е�Ԫ�ض��ǽ���Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������谷�¼���ʹ�й���ҵ����������Ӱ֮�У����Ѳ��븴�ա������谷��������[����ʽΪC3N3(NH2)3����Է���������126]��һ�ֵͶ��Ի�����Ʒ��Ӥ�������������������ϵͳ�������й������谷˵����ȷ����(����)
A. 2.52 g�����谷����ԭ����ĿΪ0.12NA
B. ��״���£�1 mol�����谷�����Ϊ22.4 L
C. �����谷������ԼΪ10%
D. �����谷��Ħ������Ϊ126 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ķ��뷽���ٹ��ˣ��������������ܷ�Һ������ȡ���������ѡ�����и������ķ��뷽��������ţ�
(1)ʳ��ˮ����ɳ______
(2)����ˮ______
(3)����ˮ����ȡ_______
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ�ÿ��ת���ڸ�����������һ��ʵ���ҽϺ������� �� ��
A. ![]()
B. ![]()
C. ![]()
D. ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ظ����ι㷺������������Ƥ�������ȡ��Ը���ʯ����Ҫ�ɷ���Cr2O3����FeO��Al2O3�� SiO2������)Ϊԭ����ȡ�ظ����Ƶ��������£�

��ش��������⣺
(1) ���������Ҫ�Ǻ�________Ԫ�ص������
(2)д��Cr2O3�봿���ڸ��±���ʱ��Ӧ�Ļ�ѧ����ʽ_______________________��
(3)���±��պ�����Ŀ����_____________________________������pHʱ�γɵij����ijɷ���_______________________________________________��
(4)д�������ữʹNa2CrO4ת��ΪNa2Cr2O7�����ӷ���ʽ ______________________��
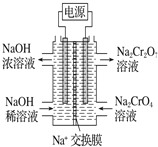
(5)ij��������ʯī�缫���Na2CrO4��Һ��ʵ ���� Na2CrO4��Na2Cr2O7��ת������ԭ����ͼ��ʾ��д�������ĵ缫��Ӧʽ____________________��
(6)Na2Cr2O7�����ڲⶨ��ˮ�Ļ�ѧ����������COD��ָÿ��ˮ���л�ԭ�����ʱ����� ����ҪO2��������������ijˮ��100��00 mL���ữ�����C1 mol/L��Na2Cr2O7��Һ V1 mL��ʹˮ�еĻ�ԭ��������ȫ��������Cr2O72����ԭΪCr3+��������C2mol/L��FeSO4��Һ�ζ�ʣ���Cr2O72�����������FeSO4��ҺV2 mL��
�ٸ�ˮ����CODΪ________________mg/L��
�ڼ���������Ӧ��������Һ��Fe3+��Cr3+�����ʵ���Ũ�Ⱦ�Ϊ0��1 mol/L��ҪʹFe3 +�� ����ȫ��Cr3+��δ��ʼ���������������ҺpH�ķ�Χ��______________��(�����õ������ݣ�KSPFe(OH)3=4��0��10-38, KSPCr(OH)3=6��0��10-31��![]() ��
��![]() ��
��![]() ��
��![]() )
)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com