
【题目】乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请回答下列问题。
(1)乙烯的电子式_______________________,结构简式____________________。
(2)鉴别甲烷和乙烯的试剂是_____________(填序号)。
A 稀硫酸 B 溴的四氯化碳溶液
C 水 D 酸性高锰酸钾溶液
(3)下列物质中,可以通过乙烯加成反应得到的是___________(填序号)。
A CH3CH3 B CH3CHCl2
C CH3CH2OH D CH3CH2Br
(4)工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为____________________________________,反应类型是______________。
【答案】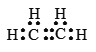 H2C=CH2 BD ACD nCH2=CH2
H2C=CH2 BD ACD nCH2=CH2![]()
![]() 加聚反应
加聚反应
【解析】
(1)乙烯是含有碳碳双键的最简单的烯烃,分子式为C2H4;
(2)乙烯分子中含有碳碳双键,可以发生加成反应,可以被强氧化剂氧化,而甲烷不能;
(3)乙烯加成反应的特征是原子或原子团加在双键碳原子上,双键变为单键;
(4)一定条件下,乙烯可以发生加聚反应生成聚乙烯。
(1)(1)乙烯的分子式为C2H4,分子中含有碳碳双键,结构简式为H2C=CH2,电子式为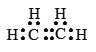 ;
;
(2)乙烯分子中含有碳碳双键,可以与溴水发生加成反应,使溴水褪色,可以与强氧化剂酸性高锰酸钾溶液发生氧化反应,使酸性高锰酸钾弱于褪色,而甲烷不能,则鉴别甲烷和乙烯的试剂是溴水和酸性高锰酸钾溶液,故答案为:BD;
(3)乙烯分子中含有碳碳双键,一定条件下,乙烯和氢气发生加成生成乙烷,和氯气反应生成1,2—二氯乙烷,和水发生加成生成乙醇,溴化氢发生加成生成溴乙烷,ACD正确,故答案为:ACD;
(4)一定条件下,乙烯发生加聚反应生成合成有机高分子化合物聚乙烯,反应的化学方程式为nCH2=CH2![]()
![]() ,是加聚反应。
,是加聚反应。


科目:高中化学 来源: 题型:
【题目】氰气的化学式为(CN)2,结构式为N=C—C=N,性质与卤素相似。下列叙述正确的是( )
A.不和氢氧化钠溶液发生反应
B.分子中键的键长大于C≡C键的键长
C.分子中含有2个σ键和4个π键
D.分子中既有极性键,又有非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:X(s)+Y(g)![]() 2Z(g)在容积为1L密闭容器反应,下列叙述不是反应达到平衡状态的标志的是
2Z(g)在容积为1L密闭容器反应,下列叙述不是反应达到平衡状态的标志的是
①单位时间内生成1molX的同时消耗2molZ ②Z的体积分数不再变化
③体系的压强不再改变 ④Y、Z的物质的量浓度比为1:2
⑤Y的转化率不再改变的状态 ⑥混合气体的密度不再改变的状态
A. 仅①④ B. ①③④ C. ①④⑤ D. ②③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列几组物质:
①金刚石与C60 ②16O和18O ③![]() 和
和![]()
④CH4和CH3CH2CH3 ⑤CH2![]() CH2和CH2
CH2和CH2![]() CH—CH
CH—CH![]() CH2
CH2
⑥ 和
和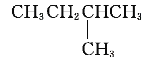
⑦(CH3)2CHCH3和
(1)互为同位素的是_______(填序号,下同)。
(2)互为同分异构体的是_______。
(3)互为同系物的是_______。
(4)互为同素异形体的是_______。
(5)属于同一种物质的是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯广泛用于药物、燃料、香料等工业,在中学化学实验室里常用下图装置来制备乙酸乙酯。(部分夹持仪器已略去)

已知:

制备粗品(图1)
在A 中加入少量碎瓷片,将三种原料依次加入A 中,用酒精灯缓慢加热,一段时间后在B 中得到乙酸乙酯粗品。
①浓硫酸、乙醇、乙酸的加入顺序是________________________________________,A 中发生反应的化学方程式是__________________________________________。
②A 中碎瓷片的作用是_____________________________________,长导管除了导气外,还具有的作用是_____________________________。
③B 中盛装的液体是_____________________,收集到的乙酸乙酯在_________层(填“上”或“下”)。
制备精品(图2)
将B 中的液体分液,对乙酸乙酯粗品进行一系列除杂操作后转移到C 中,利用图2 装置进一步操作即得到乙酸乙酯精品。
①C 的名称是___________________。
②实验过程中,冷却水从_________口进入(填字母);收集产品时,控制的温度应在________℃左右。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯。在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题。
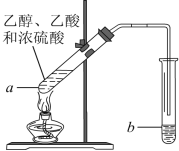
(1)乙醇分子中官能团的名称是________________。
(2)试管a中加入几块碎瓷片的目的是_________。
(3)试管a中发生反应的化学方程式为___________________________________________,反应类型是____________________。
(4)反应开始前,试管b中盛放的溶液是_______________。
(5)可用____________的方法把制得的乙酸乙酯分离出来。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库。下图是人类从海水资源获取某些重要化工原料的流程示意图。
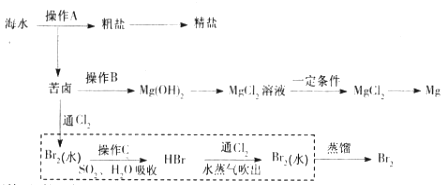
回答下列问题:
(1)操作A是_______________(填实验基本操作名称)。要知道海水晒盐的过程中溶液里食盐含量在逐渐提高的简易方法是__________________。
a.分析氯化钠含量 b.测定溶液密度 c.观察是否有沉淀析出
(2)操作B需加入下列试剂中的一种,最合适的是_____________。
a.氢氧化钠溶液 b.澄清石灰水 c.石灰乳d.碳酸钠溶液
(3)上图中虚线框内流程的主要作用是_____________。写出溴水中通入SO2时反应的离子方程式____________
(4)上图中虚线框内流程也可用![]() Br2与Na2CO3反应的化学方程式补充完整:
Br2与Na2CO3反应的化学方程式补充完整:
![]() ___________
___________
(5)已知苦卤的主要成分如下:

理论上,1 L苦卤最多可得到Mg(OH)2的质量为________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对文中描述内容的相关解释正确的是( )
选项 | 描述 | 解铎 |
A | 丹砂烧之成水银,积变又还成丹砂 | 两个反应互为可逆反应 |
B | 凡埏泥造瓦,掘地二尺余,择取无沙粘土而为之 | 其中“瓦”的主要成分为硅酸盐 |
C | 硝石(KNO3)如握盐雪不冰,强烧之,紫青烟起 | 产生“紫青烟”的原因为KNO3分解 |
D | 其法用浓酒精和槽入瓶,蒸令气上,用器承滴露 | 其中涉及的操作方法为蒸发浓缩 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,向100mL含氯化氢14.6g的盐酸溶液中,放入5.6g纯铁粉,反应进行到2min末收集到氢气1.12 L(标准状况),在此后又经过4min,铁粉完全溶解。若不考虑溶液体积的变化,则:
(1)前2min内用FeCl2表示的平均反应速率是______________。
(2)后4min内用HCl表示的平均反应速率是________________。
(3)前2min与后4min相比,反应速率__________较快,其原因是__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com