
【题目】下列表示化学反应的离子方程式,其中正确的是:( )
A.NH4HSO3溶液与足量NaOH溶液共热:NH4++HSO3﹣+2OH﹣ ![]() ?NH3↑+SO32﹣+2H2O
?NH3↑+SO32﹣+2H2O
B.向氯化铝溶液中加入过量氨水:Al3++4NH3?H2O═AlO2﹣+4NH4++2H2O
C.大理石溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O
D.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液Fe2++2H++H2O2═Fe3++2H2O
【答案】A
【解析】解:A.NH4HSO3溶液与足量NaOH溶液混合加热的离子反应为NH4++HSO3﹣+2OH﹣ ![]() NH3↑+SO32﹣+2H2O,故A正确; B.向氯化铝溶液中加入过量氨水,离子方程式:Al3++3NH3 . H2O=Al(OH)3↓+3NH4+ , 故B错误;
NH3↑+SO32﹣+2H2O,故A正确; B.向氯化铝溶液中加入过量氨水,离子方程式:Al3++3NH3 . H2O=Al(OH)3↓+3NH4+ , 故B错误;
C.大理石溶于醋酸,离子方程式:CaCO3+2CH3COOH═Ca2++CO2↑+H2O+2CH3COO﹣ , 故C错误;
D.硫酸亚铁溶液中加过氧化氢溶液的离子方程式:2Fe2++H2O2+2H+═2Fe3++2H2O,故D错误;
故选:A.
A.NH4HSO3完全反应,生成氨气、水、亚硫酸钠;
B.不符合反应客观事实;
C.醋酸为弱电解质,应保留化学式;
D.发生氧化还原反应生成硫酸铁和水,电子、电荷不守恒;


 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案科目:高中化学 来源: 题型:
【题目】“酒是陈的香”,就是因为酒在储存过程中生成了有香 味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯.
回答下列问题: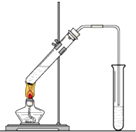
(1)写出制取乙酸乙酯的化学反应方程式
(2)饱和碳酸钠溶液的主要作用是、、 .
(3)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是 .
(4)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 .
(5)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知工业上真空炼铷的反应方程式为:2RbCl+Mg ![]() MgCl2+2Rb(g),对于此反应,能够进行正确解释的是( )
MgCl2+2Rb(g),对于此反应,能够进行正确解释的是( )
A.铷比镁金属性强
B.氯化镁比氯化铷难溶
C.高温下,镁离子得电子能力比铷离子弱
D.铷的沸点比镁低,当把铷蒸气抽走时,平衡向右反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在研究原子核外电子排布与元素周期表的关系时,人们发现价电子层相似的元素集中在一起。据此,人们将元素周期表分为5个区,如图所示。
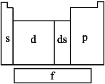
(1)在s区中,族序数最大、原子序数最小的元素是 ,其原子的外围电子的电子云形状为 。
(2)在d区中,族序数最大、原子序数最小的元素是 ,其常见离子的电子排布式为 ,其中较稳定的是 。
(3)在ds区中,族序数最大、原子序数最小的元素是 ,其原子的价电子层为 。
(4)在p区中,第二周期第ⅤA族元素原子的外围电子排布图为 。
(5)当今常用于核能开发的元素是铀和钚,它们在周期表中位于 区。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(s)C(g);△H<0,在其他条件不变时,改变其中一个条件,则生成C的速率(填“加快”、“减慢”或“不变”):
(1)升温;
(2)加正催化剂;
(3)增大容器容积;
(4)加入A;
(5)加入C .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于钠的说法不正确的是( )
A. 金属钠与O2反应,条件不同,产物不同
B. 钠—钾合金可作原子反应堆的导热剂
C. 钠着火不能用泡沫灭火器灭火,常用沙子盖灭
D. 钠性质活泼,能从盐溶液中置换出金属活动性顺序表中钠后面的金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度下2L密闭容器中,3种气体加入起始状态和平衡状态时的物质的量(n)如下表所示:
X | Y | W | |
起始状态(mol) | 2 | 1 | 0 |
平衡状态(mol) | 1 | 0.5 | 1.5 |
下列有关说法正确的是( )
A.该温度下,该反应的平衡常数K=9
B.升高温度,若W的体积分数减小,此反应△H>0
C.该温度下,该反应的方程式为 2X(g)+Y(g)3W(g)
D.增大压强,正、逆反应速率都增大,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定某有机化合物A的结构,进行如下实验:
(一)分子式的确定:
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4 g H2O和8.8 g CO2,消耗氧气6.72 L(标准状况下),则该物质中各元素的原子个数比是_________________。
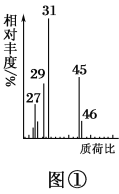
(2)用质谱仪测定该有机化合物的相对分子质量,得到如图①所示质谱图,则其相对分子质量为________,该物质的分子式是________。
(3)根据价键理论,预测A的可能结构并写出结构简式________。
(二)结构式的确定:
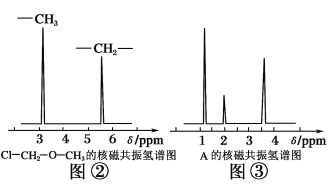
(4)核磁共振氢谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目。例如:甲基氯甲基醚(Cl—CH2—O—CH3)有两种氢原子如图②。经测定,有机物A的核磁共振氢谱示意图如图③,则A的结构简式为__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com