
【题目】利用某分子筛作催化剂,NH3可脱除废气中的NO和NO2,生成两种无毒物质,其反应历程如下图所示,下列说法正确的是( )
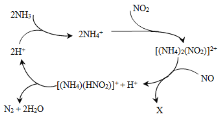
A.X是N2
B.汽车尾气中含有的氮氧化合物是由于汽油燃烧产生的
C.NH4+中含有非极性共价键
D.上述历程的总反应为:2NH3+NO +NO2 2N2+3H2O
2N2+3H2O
科目:高中化学 来源: 题型:
【题目】现有下列9种微粒:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 。按要求完成以下各题:
。按要求完成以下各题:
(1)![]() 、
、![]() 分别是氢元素的一种______,它们互为______。
分别是氢元素的一种______,它们互为______。
(2)互为同素异形体的微粒是______。
(3)![]() 的中子数为______,核外电子数为______。
的中子数为______,核外电子数为______。
(4)形成上述9种微粒的核素有______种、元素有______种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A.少量的碳酸氢钠溶液与澄清石灰水混合:2![]() +2OH-+Ca2+=CaCO3↓+
+2OH-+Ca2+=CaCO3↓+![]() +2H2O
+2H2O
B.过量的碳酸氢钠溶液与澄清石灰水混合:![]() +OH-+Ca2+=CaCO3↓+H2O
+OH-+Ca2+=CaCO3↓+H2O
C.碳酸氢钠溶液与少量的盐酸溶液混合:![]() +H+=CO2↑+H2O
+H+=CO2↑+H2O
D.碳酸钠溶液与过量的盐酸溶液混合:Na2CO3+2H+=2Na++CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在周期表中的相对位置如图所示,已知它们的最外层电子数之和为21,下列说法错误的是( )
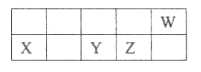
A. 原子半径由大到小的顺序:X、Y、Z、W
B. 元素最高正价由低到高的顺序:X、Y、Z、W
C. 简单氢化物的热稳定性由弱到强的顺序:Y、Z、W
D. 最高价氧化物的水化物的酸性由弱到强的顺序:X、Y、Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
钛镍形状记忆合金(TiNi)被广泛用于人造卫星和宇宙飞船的天线,在临床医疗领域内也具有广泛的应用。回答下列问题:
(1)写出基态Ti原子的电子排布式:_________,Ni在元素周期表中的位置是_________。
(2)钛镍合金能溶于热的硫酸生成Ti(SO4)2、NiSO4,二者阴离子的立体构型为______,中心原子的轨道杂化类型是_______。
(3)工业上将金红石(主要成分TiO2)转化为液态TiCl4,再用金属镁在高温下还原得到金属钛,同时生成MgCl2。
①MgCl2的熔沸点比TiCl4高得多,其原因是______。
②原子半径r(Cl)_____r(Mg),离子半径r(O2-)______r(Mg2+)(填“>”、“<”或“=”)。
(4)金属镍能与CO反应生成一种配合物Ni(CO)4(常温下为无色液体)。Ni(CO)4的固体属于_____晶体,Ni与CO之间的化学键称为__________,提供孤对电子的成键原子是_________。(填元素符号)
(5)一种钛镍合金的立方晶胞结构如图所示:
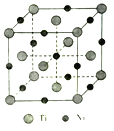
①该合金中Ti的配位数为________。
②若合金的密度为d g/cm3,晶胞边长a=________pm。(用含d的计算式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有某铁碳合金(可以看作铁和碳两种单质的混合物),化某学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了如图所示的实验装置(夹持仪器已省略)和实验方案进行实验探究。
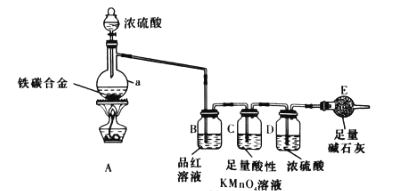
请回答下列问题:
(1)仪器 a 的名称是________________。
(2)连接好装置后,首先应进行的操作是 _____________
(3)向仪器a中滴加足量的浓硫酸,未点燃酒精灯前,A、B、C三装置中均无明显现象,其原因是___________、_______________ 。
(4)仪器a中铁与浓硫酸发生反应的化学方程式是____________ 。
(5)装置C中发生的反应中,SO2体现_________性。
(6)实验开始前,甲同学称量装置 E 的质量,并将m g铁碳合金样品放入仪器 a 中,再加入足量的浓硫酸,待仪器a中不再逸出气体时,停止加热,拆下装置E并称重,装置E增重n g。据此甲同学计算铁碳合金中铁的质量分数为________________(写表达式)。
(7)乙同学认为,依据此实验测得的数据,计算得到的铁碳合金中铁的质量分数可能会偏低,原因是空气中的CO2、H2O进入装置E中使n增大。你认为改进的方法是_____________。
(8)丙同学认为 ,即使乙同学认为的偏差得到改进 ,依据此实验测得的铁碳合金中铁的质量分数也可能仍会有误差。 你认为其中的原因是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】U、V、W、X、Y、Z 是原子序数依次增大的六种常见元素。Y 的单质在 W2 中 燃烧的产物可使品红溶液褪色 。 Z 和 W元素形成的化合物 Z3W4 具有磁性 。 U 的单质在 W2中燃烧可生成 UW 和 UW2 两种气体 。 X 的单质是一种金属,与冷水反应缓慢、与沸水反应迅速。
请回答下列问题:
(l)V的单质的分子式为____________ 。
(2)Z元素在周期表中的位置是____________。
(3)U、V、W形成的10电子氢化物中,沸点最高的是_________(填化学式,下同);V、W 的简单氢化物分子结合H+能力较强的是_________。
(4)X和Y元素形成的化合物的电子式为___________。
(5)Y的最高价氧化物对应的水化物与X单质反应的离子方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加徳罗常数的值,下列说法正确的是
A.常温下,1L pH=13的Ba(OH)2溶液中OH-数目为0.2NA
B.在电解精炼粗铜的过程中,当阴极质量增重32 g时转移电子数目为NA
C.常温常压下,1 mol分子式为C2H6O的有机物中,含有C—O键的数目为NA
D.氢氧燃料电池正极消耗22.4L气体时,负极消耗的气体分子数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“探险队员”——硫酸,不小心走进了有许多“吃人的野兽”如图所示(即能与硫酸发生化学反应的物质)的小山,逃生线路有多种,但有一种线路是完全行不通,处处为陷阱,即为入口→③→⑤→⑦→⑨→出口,则该线路涉及的物质为( )

A.Na2CO3、Fe(OH)3、Zn、Fe2O3B.SO3、Cu、BaCl2、HCl
C.Zn、Fe(OH)3、KNO3、CuOD.SO3、Cu、NaCl、CuO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com