
【题目】U、V、W、X、Y、Z 是原子序数依次增大的六种常见元素。Y 的单质在 W2 中 燃烧的产物可使品红溶液褪色 。 Z 和 W元素形成的化合物 Z3W4 具有磁性 。 U 的单质在 W2中燃烧可生成 UW 和 UW2 两种气体 。 X 的单质是一种金属,与冷水反应缓慢、与沸水反应迅速。
请回答下列问题:
(l)V的单质的分子式为____________ 。
(2)Z元素在周期表中的位置是____________。
(3)U、V、W形成的10电子氢化物中,沸点最高的是_________(填化学式,下同);V、W 的简单氢化物分子结合H+能力较强的是_________。
(4)X和Y元素形成的化合物的电子式为___________。
(5)Y的最高价氧化物对应的水化物与X单质反应的离子方程式为__。
【答案】N2 第四周期第VIII族 H2O NH3 Mg2+![]() Mg+2H+=Mg2++H2↑
Mg+2H+=Mg2++H2↑
【解析】
U、V、W、X、Y、Z是原子序数依次增大的六种常见元素。Z和W元素形成的化合物Z3W4具有磁性,则Z3W4为Fe3O4,Z为Fe元素,W为O元素。Y的单质在W2中燃烧的产物可使品红溶液褪色,该产物为SO2,则Y为S元素;U的单质在W2中燃烧可生成UW和UW2两种气体,U原子序数小于O元素,应为CO和CO2气体,U为C元素;X的单质是一种金属,与冷水反应缓慢、与沸水反应迅速,则X为Mg元素;V的原子序数介于碳、氧之间,则V为N元素。由上述分析可知,U为C、V为N、W为O、X为Mg、Y为S、Z为Fe。
(1)V的单质为N2;
(2)Z为Fe,是26号元素,在周期表中的位置是:第四周期第ⅤⅢ族;
(3)U、V、W形成的10电子氢化物分别是CH4、NH3、H2O,NH3、H2O分子之间存在氢键,甲烷分子之间为范德华力,氢键比范德华力更强,常温下水为液态,故沸点最高的是H2O;NH3的水溶液呈碱性,NH3+H3O+=NH4++H2O可证明氨气与水比较更易结合H+;
(4)X和Y元素形成的化合物为硫化镁,是离子化合物,含离子键,故硫化镁的电子式为:Mg2+![]() ;
;
(5)Y的最高价氧化物对应的水化物为硫酸,X单质为镁,二者发生置换反应,反应的离子方程式:Mg+2H+=Mg2++H2↑。


科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是
A.碳酸氢铵溶液中加入足量的浓氢氧化钠溶液并加热:NH![]() +OH-
+OH-![]() NH3↑+H2O
NH3↑+H2O
B.铜与稀硝酸的反应:Cu+4H++2NO![]() =Cu2++2NO2↑+2H2O
=Cu2++2NO2↑+2H2O
C.向Ba(OH)2溶液中滴加稀硫酸:Ba2++OH-+H++SO![]() =BaSO4↓+H2O
=BaSO4↓+H2O
D.过量二氧化硫与氢氧化钠溶液反应:SO2+OH-=HSO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】RbH是一种离子化合物,它跟水反应的方程式为:![]() ,它也能跟液氨、乙醇等发生类似的反应,并都产生氢气,下列有关RbH的叙述错误的是
,它也能跟液氨、乙醇等发生类似的反应,并都产生氢气,下列有关RbH的叙述错误的是![]()
A.灼烧RbH时,火焰有特殊颜色
B.RbH中![]() 半径比
半径比![]() 半径小
半径小
C.跟液氨反应时,有![]() 生成
生成
D.在Na、K、Rb三种单质中,Rb的熔点最低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用某分子筛作催化剂,NH3可脱除废气中的NO和NO2,生成两种无毒物质,其反应历程如下图所示,下列说法正确的是( )
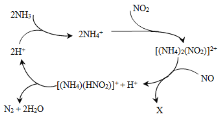
A.X是N2
B.汽车尾气中含有的氮氧化合物是由于汽油燃烧产生的
C.NH4+中含有非极性共价键
D.上述历程的总反应为:2NH3+NO +NO2 2N2+3H2O
2N2+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。
(1)把与下面元素有关性质相符的曲线标号填入相应的空格中:
a. 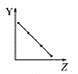 b.
b. 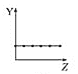 c.
c. 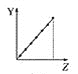 d.
d. 
①第ⅡA族元素的价电子数________。
②第三周期元素的最高化合价________。
③F-、Na+、Mg2+、Al3+的离子半径________。
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M元素原子的最外层电子数与电子层数之比为4∶3;N-、Z+、X+的半径逐渐减小;化合物XN常温下为气体。据此回答:
①X为___________(名称),Y为____________(元素符号),Z原子结构示意图为________________。
②N的最高价氧化物的水化物的化学式为________________。
③M的最高价氧化物的化学式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质有如下转化关系![]() 有的生成物未列出
有的生成物未列出![]() ,其中:D为碱,G为酸,金属甲在G 的浓溶液中会钝化;F的溶液中只含一种溶质.
,其中:D为碱,G为酸,金属甲在G 的浓溶液中会钝化;F的溶液中只含一种溶质.
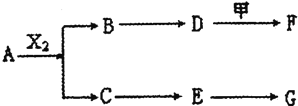
A、B、C、D、E均由Q、R、X、T四种短周期元素中的两种或三种组成,且Q、R、X、T原子序数依次增大;X的最外层电子数是电子层数的3倍;R和X相邻;Q和T同主族,Q为非金属元素,T为金属元素.则:
(1)X在周期表中的位置是 ______ ,R、X、T的原子半径从小到大的顺序为 ______ ![]() 用元素符号表示
用元素符号表示![]() ;
;
(2)A和G等物质的量反应产物的水溶液显 ______ 性,其原因用离子方程式表示为 ______ ;
(3)A和X2反应的化学方程式为 ______ ;
(4)pH均为12的D溶液和F溶液中,水电离出的c(OH-)之比为 ______ ;
(5)为保护环境,通过安装汽车尾气处理装置,使尾气中的E和CO反应转化为两种空气的成分,当反应转移1 mol电子时,生成的气体在标准状况下的总体积为 ______ L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某厂利用一种天然产物进行发酵,发现发酵液中含有U、V、W、X等多种化合物。已知:①U和W均可与银氨溶液反应,析出金属银,而且U是一种单糖。②V是单官能团化合物,其碳原子数和X相同。V在浓硫酸作用下经加热得到Y,Y可以使溴水褪色。③V经缓和氧化可生成W。④V和X在少量浓硫酸作用下经加热可以得到Z。⑤X的组成为C 40%、H 6.7%、O 53.3%,X含有一个羧基,已知X的相对分子质量为90。X也可与乙酸起酯化反应。根据上述条件,回答下列问题:
(1)写出符合U的一种可能的单糖结构简式:___________。
(2)X的分子式是_____,其所有可能的结构简式是_________。
(3)V、W、Y、Z的可能的结构简式分别是:V_____,W_____,Y_______,Z______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙烯是一种重要的有机化工原料,其结构简式为![]() ,它一般不可能具有的性质是
,它一般不可能具有的性质是
A. 易溶于水,不易溶于有机溶剂
B. 在空气中燃烧产生黑烟
C. 能使溴的四氯化碳溶液褪色,也能使酸性高锰酸钾溶液褪色
D. 能发生加成反应,在一定条件下可与4倍物质的量的氢气加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. CH3(C2H5)CHCH(CH3)2的系统命名为2—甲基—3—乙基丁烷
B. 苯甲酸的结构简式为![]()
C. 利用乙醇的还原性以及Cr3+、Cr2O72-的颜色差异来检验酒后驾车
D. C5H10的同分异构体中属于烯烃的有6种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com