
【题目】某厂利用一种天然产物进行发酵,发现发酵液中含有U、V、W、X等多种化合物。已知:①U和W均可与银氨溶液反应,析出金属银,而且U是一种单糖。②V是单官能团化合物,其碳原子数和X相同。V在浓硫酸作用下经加热得到Y,Y可以使溴水褪色。③V经缓和氧化可生成W。④V和X在少量浓硫酸作用下经加热可以得到Z。⑤X的组成为C 40%、H 6.7%、O 53.3%,X含有一个羧基,已知X的相对分子质量为90。X也可与乙酸起酯化反应。根据上述条件,回答下列问题:
(1)写出符合U的一种可能的单糖结构简式:___________。
(2)X的分子式是_____,其所有可能的结构简式是_________。
(3)V、W、Y、Z的可能的结构简式分别是:V_____,W_____,Y_______,Z______。
【答案】CH2OH(CHOH)4CHO或CH2OH(CHOH)3COCH2OH C3H6O3 HOCH2CH2COOH或CH3CH(OH)COOH CH3CH2CH2OH CH3CH2CHO CH3CH=CH2 HOCH2CH2COOCH2CH2CH3或CH3CH(OH)COOCH2CH2CH3
【解析】
U是一种单糖,能发生银镜反应,可能为葡萄糖。X分子中C、H、O原子数目之比为![]() ,X最简式为CH2O,X可以表示为(CH2O)n,X的相对分子质量为90,则
,X最简式为CH2O,X可以表示为(CH2O)n,X的相对分子质量为90,则![]() ,可知X分子式为C3H6O3,X含有一个羧基,X也可与乙酸起酯化反应,则X含有羟基,X结构简式为HOCH2CH2COOH或CH3CH(OH)COOH。V在浓H2SO4作用下加热生成Y,Y可以使溴水褪色,则Y属烯烃,V是醇,而V是单官能团化合物,其碳原子数与X相同,V经缓和氧化可生成W,W可以与银氨溶液反应,含有-CHO,则V含有-CH2OH结构。则V是CH3CH2CH2OH,Y是CH3CH=CH2,W为CH3CH2CHO。V和X在浓H2SO4作用下生成Z,则Z属于酯类,为HOCH2CH2COOCH2CH2CH3或CH3CH(OH)COOCH2CH2CH3。
,可知X分子式为C3H6O3,X含有一个羧基,X也可与乙酸起酯化反应,则X含有羟基,X结构简式为HOCH2CH2COOH或CH3CH(OH)COOH。V在浓H2SO4作用下加热生成Y,Y可以使溴水褪色,则Y属烯烃,V是醇,而V是单官能团化合物,其碳原子数与X相同,V经缓和氧化可生成W,W可以与银氨溶液反应,含有-CHO,则V含有-CH2OH结构。则V是CH3CH2CH2OH,Y是CH3CH=CH2,W为CH3CH2CHO。V和X在浓H2SO4作用下生成Z,则Z属于酯类,为HOCH2CH2COOCH2CH2CH3或CH3CH(OH)COOCH2CH2CH3。
(1)根据分析,U可能为葡萄糖,其结构简式为CH2OH(CHOH)4CHO,也可能是果糖,结构简式为CH2OH(CHOH)3COCH2OH;
(2)X的分子式为C3H6O3,可能的结构简式为HOCH2CH2COOH或CH3CH(OH)COOH;
(3)根据分析,V的结构简式为CH3CH2CH2OH,W的结构简式为CH3CH2CHO,Y的结构简式为CH3CH=CH2,Z的结构简式为HOCH2CH2COOCH2CH2CH3或CH3CH(OH)COOCH2CH2CH3。


科目:高中化学 来源: 题型:
【题目】回答下列问题
![]() 工业利用冶铜炉渣
工业利用冶铜炉渣![]() 含Fe2O3、FeO、SiO2、Al2O3等
含Fe2O3、FeO、SiO2、Al2O3等![]() 制Fe2O3的生产流程示意图如下:
制Fe2O3的生产流程示意图如下:
炉渣![]() 滤液
滤液![]() 沉淀
沉淀![]() 氧化铁
氧化铁
经“足量的NaOH溶液”处理后,铝元素的存在形态为 ______ ![]() 填序号
填序号![]() .
.
a.Al b.Al(OH)3 c.Al3+ d.AlO2-
![]() 要证明某溶液不含Fe3+但可能含有Fe2+,最佳的实验操作顺序是 ______
要证明某溶液不含Fe3+但可能含有Fe2+,最佳的实验操作顺序是 ______ ![]() 填序号
填序号![]() .
.
①加入少量氯水②加入足量KMnO4溶液③加入少量NH4SCN溶液
a. ①③ b.③② c. ③① d. ①②③
(3)25℃时,23gC2H5OH在血液中被氧气完全氧化放出668kJ热量,该反应的热化学方程式为 ______ .
(4)X、Y、Z、Q、R是原子序数依次增大的短周期主族元素,X、Q同主族,Z+与Y2-具有相同的电子层结构,Q 的单质是一种重要的半导体材料,R的单质在常温下呈气态.
①X、Y、Z三种元素的原子半径从大到小的顺序是 ______ ![]() 用元素符号表示
用元素符号表示![]() ,写出含有X、Y、Z三种元素且水溶液显碱性的物质化学式 ______ .
,写出含有X、Y、Z三种元素且水溶液显碱性的物质化学式 ______ .
![]() 下列选项一定能说明R的非金属性比X强的是 ______
下列选项一定能说明R的非金属性比X强的是 ______ ![]() 填序号
填序号![]() .
.
a.原子的半径:r(R)>r(X)
b.原子的最外层电子数:n(R)>n(X)
c.热稳定性:R的气态氢化物>X的气态氢化物
d.酸性:R的最高价氧化物对应的水化物>X的最高价氧化物对应的水化物
③R在周期表的位置是 ______ R和Q形成的化合物在潮湿的空气中冒白色烟雾,该反应的化学方程式为 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
钛镍形状记忆合金(TiNi)被广泛用于人造卫星和宇宙飞船的天线,在临床医疗领域内也具有广泛的应用。回答下列问题:
(1)写出基态Ti原子的电子排布式:_________,Ni在元素周期表中的位置是_________。
(2)钛镍合金能溶于热的硫酸生成Ti(SO4)2、NiSO4,二者阴离子的立体构型为______,中心原子的轨道杂化类型是_______。
(3)工业上将金红石(主要成分TiO2)转化为液态TiCl4,再用金属镁在高温下还原得到金属钛,同时生成MgCl2。
①MgCl2的熔沸点比TiCl4高得多,其原因是______。
②原子半径r(Cl)_____r(Mg),离子半径r(O2-)______r(Mg2+)(填“>”、“<”或“=”)。
(4)金属镍能与CO反应生成一种配合物Ni(CO)4(常温下为无色液体)。Ni(CO)4的固体属于_____晶体,Ni与CO之间的化学键称为__________,提供孤对电子的成键原子是_________。(填元素符号)
(5)一种钛镍合金的立方晶胞结构如图所示:
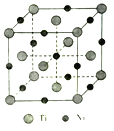
①该合金中Ti的配位数为________。
②若合金的密度为d g/cm3,晶胞边长a=________pm。(用含d的计算式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】U、V、W、X、Y、Z 是原子序数依次增大的六种常见元素。Y 的单质在 W2 中 燃烧的产物可使品红溶液褪色 。 Z 和 W元素形成的化合物 Z3W4 具有磁性 。 U 的单质在 W2中燃烧可生成 UW 和 UW2 两种气体 。 X 的单质是一种金属,与冷水反应缓慢、与沸水反应迅速。
请回答下列问题:
(l)V的单质的分子式为____________ 。
(2)Z元素在周期表中的位置是____________。
(3)U、V、W形成的10电子氢化物中,沸点最高的是_________(填化学式,下同);V、W 的简单氢化物分子结合H+能力较强的是_________。
(4)X和Y元素形成的化合物的电子式为___________。
(5)Y的最高价氧化物对应的水化物与X单质反应的离子方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.苯酚钠的溶液中通入过量CO2:2![]() +CO2+H2O→CO32-+2
+CO2+H2O→CO32-+2![]()
B.NaOH溶液中加入少量苯酚:C6H5OH+OH-→C6H5O-+H2O
C.银氨溶液中加入少量乙醛溶液,水浴加热:CH3CHO+2Ag(NH3)2++2OH-![]() CH3COONH4+2Ag↓+3NH3+H2O
CH3COONH4+2Ag↓+3NH3+H2O
D.乙酸钠溶液加入少量盐酸:CH3COONa+H+→CH3COOH+Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加徳罗常数的值,下列说法正确的是
A.常温下,1L pH=13的Ba(OH)2溶液中OH-数目为0.2NA
B.在电解精炼粗铜的过程中,当阴极质量增重32 g时转移电子数目为NA
C.常温常压下,1 mol分子式为C2H6O的有机物中,含有C—O键的数目为NA
D.氢氧燃料电池正极消耗22.4L气体时,负极消耗的气体分子数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应2A(s)+3B(g) ![]() C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( )
C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( )
①增加A的量,平衡向正反应方向移动
②升高温度,平衡向逆反应方向移动,v(正)减小
③压强增大一倍,平衡不移动,v(正)、v(逆)不变
④增大B的浓度,v(正)>v(逆)
⑤加入催化剂,B的转化率提高
A.①②B.④C.③D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2﹣羟基异丁酸乙酯能溶于水,是一种应用于有机合成和药物制造的化工原料。

(1)2﹣羟基异丁酸乙酯的分子式为_________,不同化学环境的氢在核磁共振氢谱图中有不同的吸收峰,则2﹣羟基异丁酸乙酯有_________个吸收峰;
(2)①②的反应类型分别为_________,_________;
(3)已知I为溴代烃,I→B的化学方程式为_________;
(4)缩聚产物F的结构简式为_________;
(5)下列关于![]() 和
和 的说法正确的有_________(双选,填字母);
的说法正确的有_________(双选,填字母);
A.后者遇到FeCl3溶液显紫色,而前者不可
B.两者都可以与NaHCO3溶液反应放出CO2
C.两者都可以与氢氧化钠溶液发生反应,当两者物质的量相等时,消耗氢氧化钠的量不相等
D.两者都可以与氢气发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图某工厂用NO气体制取NH4NO3溶液,下列说法正确的是
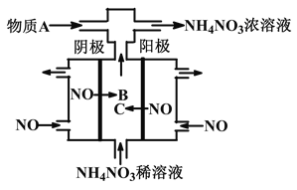
A. 阳极的电极反应式为:NO-3e-+2H2O=NO2-+4H+
B. 物质B与物质C是同一种物质
C. A物质可为氨气
D. 阴、阳两极转移的电子数之比为5∶3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com