
【题目】某研究小组为探究元素周期表中元素性质的递变规律,设计了如下实验。
Ⅰ.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:________与盐酸反应最剧烈,________与盐酸反应的速度最慢;________与盐酸反应产生的气体最多。
向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为_______________。
(3)资料显示:钠、镁、铝都可以用于制备储氢的金属氢化物。
① NaH是离子化合物,能与水发生氧化还原反应生成H2,该反应的还原剂是________________。
② NaAlH4是一种良好的储氢材料。NaAlH4与水反应产生氢气的化学方程式为____________________。
Ⅱ.为验证氯、溴、碘三种元素的非金属性强弱,用下图所示装置进行试验(夹持仪器已略去,气密性已检验)。
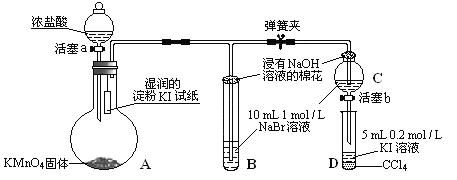
实验过程:
①打开弹簧夹,打开活塞a,滴加浓盐酸。
②当B和C中的溶液都变为黄色时,夹紧弹簧夹。
③当B中溶液由黄色变为棕红色时,关闭活塞a。
④……
(1)A中发生反应生成氯气,请写出该反应的离子方程式:___________________。
(2)验证氯气的氧化性强于碘的实验现象是________________________。
(3)B、C管口“浸有NaOH溶液的棉花”的作用是__________________________。
(4)为验证溴的氧化性强于碘,过程④的操作和现象是______________________。
(5)过程③实验的目的是____________________。
(6)请运用原子结构理论解释氯、溴、碘非金属性逐渐减弱的原因:_______________。
【答案】 钾 铝 铝 S2-+Cl2 == S↓+2Cl- NaH NaAlH4+2H2O=NaAlO2+4H2↑ 2MnO4-+16H++10Cl-== 2Mn2++5Cl2↑+8H2O 淀粉KI试纸变蓝 吸收氯气 防止污染 打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡。静止后CCl4层溶液变为紫红色 确认C的黄色溶液中无Cl2,排除Cl2对溴置换碘实验的干扰 同主族元素从上到下,原子半径逐渐增大,得电子能力逐渐减弱
【解析】Ⅰ.(1)金属活泼性顺序为:钾>钠>镁>铝,所以相同条件下与盐酸反应最激烈的是钾,反应速率最慢的是铝;生成1mol氢气需要得到2mol电子,1mol钾、钠都失去1mol电子,1mol镁失去2mol电子,而1mol铝失去3mol电子,所以生成氢气最多的是金属铝;(2)氯气氧化性强于硫单质,所以氯气能够与硫离子反应生成硫,反应的离子方程式为:S2-+Cl2═S↓+2Cl-;(3)① NaH和水反应的方程式为:NaH+H2O=NaOH+H2↑,其中水是氧化剂,NaH是还原剂;由上述反应不难发现NaAlH4中的H呈-1价,同样可以被水氧化为氢气,同时生成NaAlO2,即:NaAlH4+2H2O=NaAlO2+4H2↑;
Ⅱ.(1)A中高锰酸钾与浓盐酸反应生成氯气、氯化钾、氯化锰和水的离子方程式为:2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O;(2)验证氯气的氧化性强于碘的实验现象是KI淀粉试纸变蓝,Cl2+2I-=2Cl-+I2 ,I2遇淀粉变蓝色;(3)B、C管口“浸有NaOH溶液的棉花”的作用是:吸收氯气,防止污染空气;(4)为验证溴的氧化性强于碘,过程④的操作和现象是打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡。静止后CCl4层溶液变为紫红色,其中紫红色为I2溶解在CCl4呈现的颜色;(5)过程③实验的目的是确认C的黄色溶液中无Cl2,排除Cl2对溴置换碘实验的干扰;(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下,原子半径逐渐增大,得电子能力逐渐减弱。


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
【题目】水系锂电池具有安全、环保和价格低廉等优点成为当前电池研究领域的热点.以钒酸钠(NaV3O8)为正极材料的电极反应式为:NaV3O8+xLi++xe﹣═NaLixV3O8 , 则下列说法不正确的是( ) 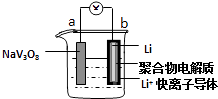
A.放电时,该电池的总反应为:xLi+NaV3O8═NaLixV3O8
B.充电过程中Li+从阳极向阴极迁移
C.充电过程中阳极的电极反应式为NaLixV3O8﹣xe﹣═NaV3O8+xLi+ , NaLixV3O8中钒的化合价发生变化
D.该电池可以用硫酸钠溶液作电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Z、Q、R、T、U分别代表原子序数依次增大的短周期元素,周期表的全部元素中X的原子半径最小,X与R的最外层电子数相等;Z的内层电子数是最外层电子数的一半,U的最高化合价和最低化合物的代数和为6;R和Q可形原子数之比为1:1和2:1的两种化合物;R、T、U三者的最高价氧化物对应的水化物两两之间能发生化学反应.请回答下列问题:
(1)T元素在期表中的位置是________;由上述元素中的四种元素形成的既含有离子键又含有共价键的化合物为________(写出其中一种物质的名称).
(2)X、Z、Q三种元素的原子半径由小到大顺序为________(填元素符号).
(3)T、U两元素最高价氧化物对应的水化物反应的离子方程式为________.
(4)下列可以判断R和T金属性强弱的是________(填序号).
a.单质的熔点R比T低 b.单质与酸反应时,失电子数R比T少
c.单质与水反应R比T剧烈 d.最高价氧化物的水化物的碱性R比T强
(5)某同学用Q、R两元素的单质反应生成固体物质R2Q2,R2Q2属于离子化合物,且能与化合物X2Q反应生成Q的单质.R2Q2的电子式为________;R2Q2与X2Q反应的化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有前四周期A、B、C、D、E、X六种元素,已知B、C、D、E、A五种非金属元素原子半径依次减小,其中B的s能级上电子总数等于p能级上电子总数的2倍.X原子的M能层上有4个未成对电子.请回答下列问题: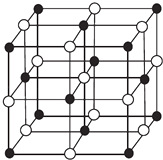
(1)写出C、D、E三种原子第一电离能由大到小的顺序为 . (用元素符号表示)
(2)A原子与B、C、D原子形成最简单化合物的稳定性由强到弱的顺序为(用分子式表示),根据价层电子对互斥理论预测BA2D的分子构型为 .
(3)某蓝色晶体,其结构特点是X2+、X3+离子分别占据六面体互不相邻的顶点,而六面体的每条棱上均有一个BC﹣ . 与A同族且相隔两个周期的元素R的离子位于立方体的恰当位置上.根据其结构特点可知该晶体的化学式为(用最简正整数表示) .
(4)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:
离子晶体 | NaCl | KCl | CaO |
晶格能/kJmol﹣1 | 786 | 715 | 3401 |
根据表格中的数据:判断KCl、MgO、TiN三种离子晶体熔点从高到低的顺序是 . MgO晶体中一个Mg2+周围和它最邻近且等距离的O2﹣有个.
(5)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和Cr2O3中,适合作录音带磁粉原料的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中错误的有
A. 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
B. 蒸馏时,应使温度计的水银球靠近蒸馏烧瓶的瓶底
C. 过滤时,玻璃棒下端在引流过程中应靠在三层滤纸处
D. 称量时,称量物放在纸上置于托盘天平左盘,砝码直接放在天平右盘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氯化银、溴化银的溶解度分别是1.5×10﹣4g和8.4×10﹣6g,将氯化银和溴化银的饱和溶液等体积混合,再加入足量浓硝酸银溶液,则发生的反应为( )
A.只有溴化银沉淀生成
B.氯化银河溴化银沉淀等量生成
C.氯化银沉淀多于溴化银沉淀
D.氯化银沉淀少于溴化银沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,PbO2 与Cr3+反应,产物是Cr2O72-和Pb2+,则与5molCr3+反应所需PbO2的物质的量为
A. 7.5mol B. 1.5mol C. 3mol D. 3.25mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】垃圾是放错地方的资源,工业废料也可以再利用.某化学兴趣小组在实验室中用废弃的含铝、铁、铜的合金制取硫酸铝溶液、硝酸铜晶体和铁红(Fe2O3).实验方案如图:
(1)写出滤液A中加入足量硫酸后所发生反应的离子方程式: .
(2)已知Fe(OH)3沉淀的pH是3~4,溶液C通过调节pH可以使Fe3+沉淀完全.下列物质中可用作调整溶液C的pH的试剂是(填序号).
A.铜粉
B.氨水
C.氢氧化铜
D.碳酸铜
(3)常温,若溶液C中金属离子均为1molL﹣1 , Ksp[Fe(OH)3]=4.0×10﹣38 , Ksp[Cu(OH)2]=2.2×10﹣20 . 控制pH=4,溶液中c(Fe3+)= , 此时Cu(OH)2沉淀生成(填“有”或“无”).
(4)将20mLAl2(SO4)3溶液与等物质的量浓度的Ba(OH)2溶液80mL混合,反应的离子方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com