
【题目】在过去,糖尿病的检测方法是把NaOH溶液和CuSO4溶液加入某病人的尿液中,微热时,如果观察到红色沉淀,说明该尿液中含有 ( )
A. 食醋 B. 白酒 C. 食盐 D. 葡萄糖
 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:
【题目】【化学-选修3:物质结构与性质】
己知铜的配合物A(结构如下图1)。请回答下列问题:
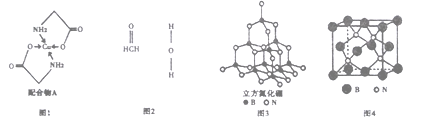
(l)Cu的简化电子排布式为_____________。
(2)A所含三种元素C、N、O的第一电离能由大到小的顺序为_________________。其中氮
原子的杂化轨道类型为_____________________。
(3)配体氨基乙酸根(H2NCH2COO-)受热分解可产生CO2和N2,N2中σ键和π键数目
之比是_____________; N2O与CO2互为等电子体,且N2O分子中O只与一个N相连,则N2O
的电子式为____________________。
(4)在Cu催化下,甲醇可被氧化为甲醛(HCHO),甲醛分子中H-C=O的键角___________1200(选填“大于”、“等于”或“小于”),甲醛能与水形成氢键,请在图2中表示出来___________。
(5)立方氮化硼(如图3)与金刚石结构相似,是超硬材料。立方氮化硼晶体内B-N键数与硼原子数之比为__________;结构化学上用原子坐标参数表示晶胞内部各原子的相对位置,图4立方氮化硼晶胞中,B原子的坐标参数分别有:B(0,0,0);B(1/2,0,1/2);B(1/2,1/2,0)等。则距离上述三个B原子最近且等距的N原子的坐标参数为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学史上每一次重大的发现都极大地推进了科学的发展。俄国科学家门捷列夫对化学的突出贡献在于
A.揭示了燃烧的本质B.开发了合成氨的生产工艺
C.提出了元素周期律D.提取了治疟药物青蒿素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为有效控制雾霾,各地积极采取措施改善大气质量。有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要。
(1)在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质。
已知:①![]() H=180.5kJ·
H=180.5kJ·![]()
②C和CO的燃烧热(H)分别为-393.5kJ·![]() 和-283kJ·
和-283kJ·![]()
则2NO(g)+2CO(g)=N2(g)+2CO2(g) H=_________kJ·![]()
(2)将0.20molNO和0.10molCO充入一个容积为1L的密闭容器中,反应过程中物质浓度变化如图所示。
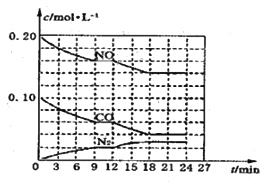
①CO在0—9min内的平均反应速率![]() =__________ mol·L-1·
=__________ mol·L-1·![]() (保留两位有效数字);第12min时改变的反应条件可能为_________。
(保留两位有效数字);第12min时改变的反应条件可能为_________。
A.升高温度 B.加入NO
C.加催化剂 D.降低温度
②该反应在第18min时又达到平衡状态,此时![]() 的体积分数为________(保留三位有效数字),化学平衡常数K=____________(保留两位有效数字)。
的体积分数为________(保留三位有效数字),化学平衡常数K=____________(保留两位有效数字)。
(3)通过人工光合作用能将水与燃煤产生的![]() 转化为HCOOH和
转化为HCOOH和![]() 。已知常温下0.1mol·
。已知常温下0.1mol·![]() 的HCOONa溶液pH=10,则HCOOH的电离常数Ka=__________。
的HCOONa溶液pH=10,则HCOOH的电离常数Ka=__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组设计的实验室制取乙酸乙酯的装置如图1所示,A中放有浓硫酸,B中放有无水乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl26C2H5OH。
②有关有机物的沸点:
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
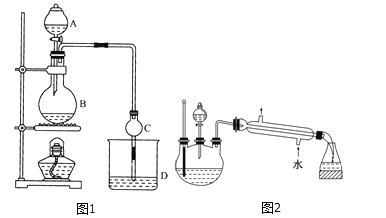
请回答:
(1)浓硫酸的作用是__________;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式:__________。
(2)球形干燥管C的作用是__________。若反应前向D中加入几滴酚酞,溶液呈红色,反应结束后D中的现象是__________。
(3)采用分液法从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,然后加入无水氯化钙,分离出__________;再加入无水硫酸钠除去水,然后进行__________(填操作名称),以得较纯净的乙酸乙酯。
(4)上述实验中饱和碳酸钠溶液的作用是______(填字母代号)。
A.反应掉乙酸和乙醇
B.反应掉乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中的更小,有利于分层析出
D.加速酯的生成,提高其产率
(5)另一化学课外小组对上述实验进行了改进,设计了图2所示的装置,利用浓硫酸、乙醇、乙酸制取乙酸乙酯(铁架台、铁夹、加热装置均已略去)与图1所示装置相比,此装置的主要优点有(写出一条即可)__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由乙烯推测丙烯(CH3CH=CH2)的结构或性质正确的是
A. 分子中3个碳原子在同一直线上
B. 分子中所有原子在同一平面上
C. 与氯化氢加成只生成一种产物
D. 能发生加聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图所示实验装置,回答下列问题:
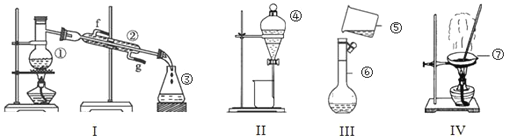
(1)写出下列仪器的名称:②_________,③_________,⑦__________。
(2)上述仪器中实验之前需检查装置是否会漏水的是______________(填仪器名称)。
(3)实验室准备用18mol/L浓硫酸配制100mL 3mol/L稀硫酸,则所需浓硫酸的体积是____mL(保留一位小数),量取浓硫酸所用量筒的规格是____(选填“10mL”、“25mL”或“50mL”)。在实验操作的摇匀过程中,不慎洒出几滴,此时应采取的措施是_______,若所配制的稀硫酸浓度偏大,则下列可能的原因分析中正确的是_______。
A.配制前,容量瓶中有少量蒸馏水 B.量取浓硫酸时,仰视液体的凹液面
C.未冷却,立即转移至容量瓶定容 D.定容时,俯视溶液的凹液面
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com