
| A、I-数目不变 | B、F-数目减少 | C、NH4+数目增大 | D、有S析出 |


 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
 (1)某混合溶液中,可能含有的离子如下表:
(1)某混合溶液中,可能含有的离子如下表:| 可能大量含有的阳离子 | H+ NH4+ Al3+ K+ Mg2+ |
| 可能大量含有的阴离子 | Cl- Br- I- CO32- AlO2- |
查看答案和解析>>
科目:高中化学 来源:湖北省荆州中学2008-2009学年上学期高一期中考试(化学) 题型:013
|
某溶液中含有K+、Mg2+、S | |
| [ ] | |
A. |
1∶1 |
B. |
4∶3 |
C. |
5∶3 |
D. |
2∶1 |
查看答案和解析>>
科目:高中化学 来源:2014届浙江省高一下学期期中考试实验班化学试卷(解析版) 题型:选择题
已知:HCO3—+AlO2—+H2O=Al(OH)3↓+CO32—某溶液中可能含有OH−,CO32−,AlO2−,SiO32−,SO42−,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示,下列说法中不正确的是
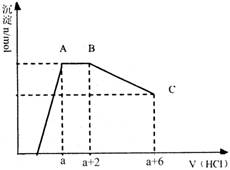
A.原溶液肯定含有OH−,CO32−,AlO2−,SiO32− B.K+和Na+至少含有其中一种
C.n(CO32−):n(AlO2−)=3:2 D.a值肯定大于4/3
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2011-2012学年浙江省余姚中学高一下学期期中考试实验班化学试卷(带解析) 题型:单选题
已知:HCO3—+AlO2—+H2O=Al(OH)3↓+CO32—某溶液中可能含有OH?,CO32?,AlO2?,SiO32?,SO42?,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示,下列说法中不正确的是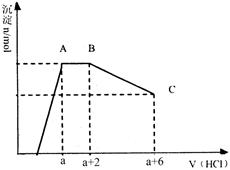
| A.原溶液肯定含有OH?,CO32?,AlO2?,SiO32? | B.K+和Na+至少含有其中一种 |
| C.n(CO32?):n(AlO2?)=3:2 | D.a值肯定大于4/3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com