
| A. | 溴酸银的溶解是一个熵增、焓减过程 | |
| B. | 对应温度下,X点的分散系中,V(溶解)>v(沉淀) | |
| C. | Y点的分散系中,c(Ag+)•c(BrO3-)>6.25×10-4 | |
| D. | 60℃时溴酸银饱和溶液中c(BrO3-)=0.025mol•L-1 |
分析 A.随着温度的升高,AgBrO3的溶解度随之增加,可判断AgBrO3的溶解过程是一个吸热反应,焓变△H>0;
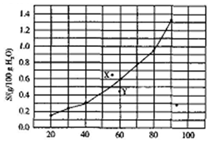
B.对应温度下,根据图象,X点时位于该温度的溶解度曲线之上,溶解曲线上的含义为J=Ksp,X点的含义为J>Ksp,据此判断化学反应的方向;
C.Y点分散系中,根据图象此时的溶度积为${K}_{sp}=6.25×{10}^{-4}$,Y点位于溶解度曲线之下,Y点的含义为J<Ksp,据此判断;
D.根据图象,60℃时,AgBrO3的溶解度为0.6g/100gH2O,据此计算溶液中$Br{O}_{3}^{-}$的浓度.
解答 解:A.AgBrO3存在沉淀溶解平衡:AgBrO3(s)?Ag+(aq)+$Br{O}_{3}^{-}(aq)$,反应是溶液中微粒数增多,体系混乱度增加,反应的熵变△S>0,随着温度的升高,AgBrO3的溶解度随之增加,可判断AgBrO3的溶解过程是一个吸热反应,焓变△H>0.故A错误.
B..对应温度下,根据图象,X点时位于该温度的溶解度曲线之上,记反应的浓度积为J,则溶解曲线上的含义为J=Ksp,X点的含义为J>Ksp,因此反应应向沉淀方向移动,则速率关系为v(溶解)<v(沉淀).故B错误.
C.Y点分散系中,根据图象此时的溶度积为${K}_{sp}=6.25×{10}^{-4}$,记反应的浓度积为J,溶解曲线上的含义为J=Ksp,Y点的含义为J<Ksp,因此溶液中c(Ag+)•$c(Br{O}_{3}^{-})$<6.25×10-4.故C错误.
D.根据图象,60℃时,AgBrO3的溶解度为0.6g/100gH2O,则溶液中$c(Br{O}_{3}^{-})$=$\frac{0.6g}{100g}=\frac{0.6g}{0.1L}=\frac{0.6}{236×0.1L}mol/L$=0.025mol/L.故D正确.
故选D.
点评 本题主要考察沉淀溶解平衡的知识,学会利用图象所传达的信息,结合浓度积与溶度积的关系判断化学反应的方向是解题的关键.题目难度不大,基础题.


 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案科目:高中化学 来源: 题型:选择题
| A. |  验证铁的吸氧腐蚀 | B. |  测定双氧水分解速率 | ||
| C. |  蒸干MgCl2溶液制备MgCl2固体 | D. |  模拟合成氨并验证有氨气生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 活化分子之间发生的碰撞一定为有效碰撞 | |
| B. | 升高温度,降低反应的活化能,可使活化分子的百分数增大,因而反应速率增大 | |
| C. | 金属腐蚀就是金属失去电子被氧化的过程 | |
| D. | 电解法精炼铜时,以粗铜作阳极,粗铜中的所有金属都以离子的形式进入电解质溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 采取低碳、节俭的生活方式 | |
| B. | 严禁排放未经处理的有毒工业废水 | |
| C. | 经常使用一次性筷子、塑料袋等 | |
| D. | 按照规定对生活废弃物进行分类放置 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应速率变化时,化学平衡一定发生移动 | |
| B. | 化学平衡发生移动时,化学反应速率一定变化 | |
| C. | 正反应进行的程度大,正反应速率一定大 | |
| D. | 化学反应速率变化而化学平衡不移动的情况,只有使用催化剂条件下才会发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Fe3+)=1 xl0-5 mol•L-1 | |
| B. | 加水稀释,平衡①向右移动 | |
| C. | 加入等体积0.2 mol•L-1KSCN溶液,溶液变为血红色 | |
| D. | 加入等体积0.2 mol•L-1CaCl2溶液,可产生沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡时压强是起始压强的$\frac{15}{14}$倍 | B. | 平衡时NH3的浓度为1 mol/L | ||
| C. | 该过程中v(O2)=0.225 mol/(L•min) | D. | 达平衡时消耗O2 1.5 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:
某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、NO3-、CO32-、Na+ | B. | NO3-、Ba2+、K+、Cl- | ||
| C. | Al3+、Ba2+、Mg2+、HCO3- | D. | NO3-、K+、SO32-、H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com