
纯碱中常含有少量的NaCl等杂质,下图仪器装置可用来测定纯碱中Na2CO3的质量分数.图中:
①空气
②某溶液
③纯碱
④某溶液
⑤碱石灰
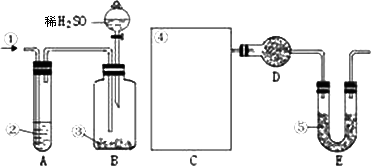
其实验步骤是:
a.按如图所示,组装好实验仪器,并检查其气密性.
b.准确称量盛有碱石灰的干燥管D的质量(设为m1 g).
c.准确称量一定量的纯碱(设为n g),并将其放入广口瓶内.
d.从分液漏斗中缓慢滴入一定量的稀硫酸,并从“①”处缓慢鼓入空气,直到B容器中不再产生气体为止.
e.准确称量干燥管D的总质量(设为m2 g).
根据上述实验回答下列问题:
(1)该实验进行到操作d时,要缓缓鼓入空气,其作用是________.装置A中盛装的液体“②”应选用________,装置A的作用是________,如果撤去装置A,直接向B中缓缓鼓入空气,则会导致实验测定结果(填“偏大”“偏小”或“不变”)________.
(2)在空白格内画出装置C及试剂④是________;装置C的作用是________;如果撤去装置C,则会导致测定结果________(填“偏大”、“偏小”或“不变”)
(3)根据此实验,计算纯碱中Na2CO3的质量分数的数学式为________(用m1、m2、n表示)
(4)装置E的作用是________.
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
 工业生产的纯碱中常含有少量的NaCl杂质.某校研究性学习活动小组为了测定混合物中纯碱的质量分数,拟使用如图实验装置(说明:连接甲和乙的橡皮管有铁夹控制),先测定一定量的样品和酸反应放出二氧化碳的质量,再计算混合物中纯碱的质量分数.
工业生产的纯碱中常含有少量的NaCl杂质.某校研究性学习活动小组为了测定混合物中纯碱的质量分数,拟使用如图实验装置(说明:连接甲和乙的橡皮管有铁夹控制),先测定一定量的样品和酸反应放出二氧化碳的质量,再计算混合物中纯碱的质量分数.| 53(w-m) |
| 22n |
| 53(w-m) |
| 22n |
查看答案和解析>>
科目:高中化学 来源: 题型:

图1-9
(A)在干燥管内填满碱石灰,总质量为m g;
(B)取n g样品装入广口瓶中;
(C)检验装置的气密性;
(D)缓缓鼓入空气数分钟,再称干燥管总质量为w g;
(E)关闭止水夹;
(F)打开止水夹;
(G)缓缓加入稀硫酸至不再产生气体为止;
(H)缓缓鼓入空气数分钟。
(1)正确的操作顺序是(填写序号):C→_______→F________→E_______→G________→D。
(2)操作步骤D中,要缓缓鼓入空气数分钟,鼓入空气的作用是________________;装置甲的作用是________________;装置乙的作用是________________。
(3)计算溶液中Na2CO3质量分数的计算式为_____________________________________。
(4)若去掉装置甲,测定结果会________;若去掉装置乙,测定结果会________。(填“偏大”“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
纯碱中常含有少量的NaCl等杂质,下图仪器装置可用来测定纯碱中Na2CO3的质量分数。
图中:①空气②某溶液③纯碱④某溶液⑤碱石灰(注:碱石灰既能吸收CO2,又能吸收H2O)
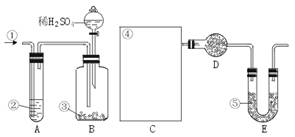 其实验步骤是:a.按上图所示,组装好实验仪器,并检查其气密性。b.准确称量盛有碱石灰的干燥管D的质量(设为m1 g)。c.准确称量一定量的纯碱(设为n g),并将其放入广口瓶内。d.从分液漏斗中缓慢滴入一定量的稀硫酸,并从“1”处缓慢鼓入空气,直到B容器中不再产生气体为止。e.准确称量干燥管D的总质量(设为m2 g)。
其实验步骤是:a.按上图所示,组装好实验仪器,并检查其气密性。b.准确称量盛有碱石灰的干燥管D的质量(设为m1 g)。c.准确称量一定量的纯碱(设为n g),并将其放入广口瓶内。d.从分液漏斗中缓慢滴入一定量的稀硫酸,并从“1”处缓慢鼓入空气,直到B容器中不再产生气体为止。e.准确称量干燥管D的总质量(设为m2 g)。
根据上述实验回答下列问题:
(1)该实验进行到操作d时,要缓缓鼓入空气,其作用是____________________ 。装置A中盛装的液体“2”应选用________________,装置A的作用是________________,如果撤去装置A,直接向B中缓缓鼓入空气,则会导致实验测定结果(填“偏大”“偏小”或“不变”)________________。
(2)在空白格内画出装置C及试剂④是__________ ;装置C的作用是________________;如果撤去装置C,则会导致测定结果________________(填“偏大”“偏小”或“不变”)
(3)根据此实验,计算纯碱中Na2CO3的质量分数的数学式为________________(用m1、m2、n表示)
(4)装置E的作用是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
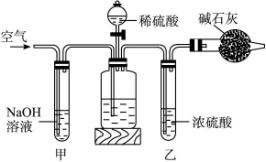
A.在干燥管内填满碱石灰,质量为m g。
B.取n g样品装入广口瓶中。
C.检验装置的气密性。
D.缓缓鼓入空气数分钟,再称干燥管质量为w g。
E.关闭止水夹。
F.打开止水夹。
G.缓缓加入稀硫酸至不再产生气体为止。
H.缓缓鼓入空气数分钟。
(1)正确的操作顺序是(填写符号):
C→________E→________→________→________→G→E→D
(2)操作步骤D中,要缓缓鼓入空气数分钟,鼓入空气的作用是__________;装置甲的作用是__________;装置乙的作用是______________________________。
(3)计算溶液中Na2CO3质量分数的计算式为______________________________。
(4)若去掉装置甲,测定结果会;若去掉装置乙,测定结果会__________。(填“偏大”“偏小”或“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
纯碱中常含有少量的NaCl等杂质,下图仪器装置可用来测定纯碱中Na2CO3的质量分数。图中:①空气②某溶液③纯碱④某溶液⑤碱石灰(注:碱石灰既能吸收CO2,又能吸收H2O)
其实验步骤是:a.按上图所示,组装好实验仪器,并检查其气密性。b.准确称量盛有碱石灰的干燥管D的质量(设为m1 g)。c.准确称量一定量的纯碱(设为n g),并将其放入广口瓶内。d.从分液漏斗中缓慢滴入一定量的稀硫酸,并从“1”处缓慢鼓入空气,直到B容器中不再产生气体为止。e.准确称量干燥管D的总质量(设为m2 g)。根据上述实验回答下列问题:

(1)该实验进行到操作d时,要缓缓鼓入空气,其作用是____________________ 。装置A中盛装的液体“2”应选用________________,
(2)在空白格内画出装置C及试剂④是______ ____ ;如果撤去装置C,则会导致测定结果________________(填“偏大”“偏小”或“不变”)
(3)装置E的作用是________________________
(4)根据此实验,计算纯碱中Na2CO3的质量分数的数学式为________________(用m1、m2、n表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com