
【题目】下列物质投入水中发生化学反应,水做氧化剂的是
A. 钠 B. 氧化钠 C. 碳酸钠 D. 过氧化钠
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案科目:高中化学 来源: 题型:
【题目】某同学称取一定质量的MgCl2固体配成溶液,在该溶液中加入一定量的稀盐酸,然后向此混合溶液中逐滴加入NaOH溶液(如下图甲所示)。滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如下图乙所示。

请回答下列问题:
(1)溶解MgCl2固体所用的玻璃仪器有______(填字母)。
a.天平 b.烧杯
c.漏斗 d.玻璃棒
(2)OA段反应的离子方程式为______________________________________。
(3)AB段反应的离子方程式为______________________________________。
(4)在B点对应的溶液中滴加AgNO3溶液,观察到的现象是________,反应的离子方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人造地球卫星上使用的一种高能电池——银锌蓄电池,其电池的电极反应式为:
Zn+2OH--2e-=ZnO+H2O,Ag2O+H2O+2e-=2Ag+2OH-。据此判断氧化银是
A.负极,被氧化 B.正极,被还原
C.负极,被还原 D.正极,被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】⑴反应N2(g)+3H2(g)2NH3(g)在恒温恒容条件下进行,下列情况中,处于平衡状态的是________;反应正向进行的是________;反应逆向进行的是_________.(填序号)
A.单位时间内消耗2mol N2,同时生成4mol NH3
B.单位时间内消耗3mol H2,同时生成2mol NH3
C.单位时间内生成2mol N2,同时生成6mol N—H键
D.混合气的密度不再随时间而改变
E.容器中气体的压强不再随时间而改变
F.单位时间内生成2mol NH3,同时又生成2mol H—H键
⑵恒温下,将amol N2与bmol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)2NH3(g)
反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,a =_________;
反应达平衡时,混合气体的体积为716.8L(标准状况下),其中NH3的体积分数为25%。平衡时NH3的物质的量为___________;
原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),n(始):n(平)=______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO和CO都是汽车尾气中的有害物质,它们缓慢起反应生成氮气和二氧化碳,即:2NO+2CO2CO2+N2,对此反应下列叙述正确的是( )
A. 使用催化剂不改变反应速率B. 降低压强,反应速率增大
C. 升高温度能加快反应速率D. 增加N2的浓度,反应速率减慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)柠檬醛 有多种同分异构体,能满足下列条件的同分异构体有_______种。
有多种同分异构体,能满足下列条件的同分异构体有_______种。
A.含有一个![]() 的六元环结构,六元环上只有一个取代基;
的六元环结构,六元环上只有一个取代基;
B.能发生银镜反应
(2)B的分子式是C4H9Cl,它与氢氧化钠的醇溶液共热,能生成两种可能的有机产物,则B的结构简式是______________________________________。
(3)实验室制备乙炔的方程式__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验安全问题的叙述中不正确的是
A. 点燃可燃性气体前需要验纯
B. 闻任何药品的气味都不能使鼻子凑近药品
C. 将水倒入浓硫酸中配制稀硫酸
D. 蒸馏液体时要放碎瓷片或沸石
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列物质:①浓硝酸、②福尔马林、③硝酸银、④硫酸铵、⑤硫酸铜、⑥氢氧化钠、⑦乙醇,其中不能使蛋白质变性的是( )
A. ①②B. ④⑤C. ④D. ④⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】S2Cl2是一种重要的化工产品。常温时是一种有毒并有恶臭的金黄色液体,熔点-76℃,沸点138℃,易与水反应,进一步氯化可得SCl2。SCl2是樱桃红色液体,易挥发,熔点-122℃,沸点59℃。SCl2 与S2Cl2相似,有毒并有恶臭,且更不稳定。S2Cl2可用下列装置制备。
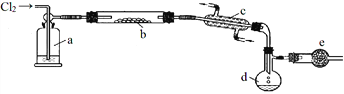
回答下列问题:
(1)写出S2Cl2的电子式________________;装置a中的试剂是________________。
(2)写出实验室制取Cl2的离子反应方程式________________________
(3)装置b中发生反应前,需进行的操作是________________________;
(4)装置e作用是___________________________;
(5)为了获得到纯净的S2Cl2,需要进行的操作名称是________________;
(6)将S2Cl2放入水中会产生沉淀和气体,写出S2Cl2与水反应的化学方程式________________。检验所产生的气体的方法是_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com