
����Ŀ���黯�أ�GaAs���������İ뵼����ϣ������������ͼ�������̫���ܵ�صIJ��ϵȣ��ش��������⣺
��1��д����̬Asԭ�ӵĺ�������Ų�ʽ ��
��2������Ԫ�������ɣ�ԭ�Ӱ뾶GaAs����һ������GaAs��������ڡ���С�ڡ���
��3��AsCl3���ӵ����幹��Ϊ �� ����As���ӻ��������Ϊ ��
��4��GaF3���۵����1000�棬GaCl3���۵�Ϊ77.9�棬��ԭ���� ��
��5��GaAs���۵�Ϊ1238�棬�ܶ�Ϊ�� gcm��3 �� �侧���ṹ��ͼ��ʾ���þ��������Ϊ �� Ga��As�������ϣ�Ga��As��Ħ�������ֱ�ΪMGa gmol��1��MAs gmol��1 �� ԭ�Ӱ뾶�ֱ�ΪrGa pm��rAs pm������٤������ֵΪNA �� ��GaAs������ԭ�ӵ����ռ��������İٷ���Ϊ �� 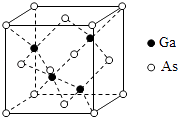
���𰸡�
��1��1s22s22p63s23p63d104s24p3
��2�����ڣ�С��
��3��������sp3
��4��GaF3Ϊ���Ӿ��壬GaCl3Ϊ���Ӿ��壬���Ӿ�����۵��
��5��ԭ�Ӿ��壻���ۣ�![]() ��100%
��100%
���������⣺��1.��AsΪ��A��33��Ԫ�أ������Ų�ʽΪ��1s22s22p63s23p63d104s24p3���Դ��ǣ�1s22s22p63s23p63d104s24p3��
��2.������Ԫ�������ɣ�Ga��Asλ��ͬһ���ڣ�Gaԭ������С��As���ʰ뾶Ga����As��ͬ���ڵ�һ�����ܴ����ң������ʵ�һ������GaС��As�����Դ��ǣ����ڣ�С�ڣ�
��3.��AsCl3�м۲���ӶԸ���=�Ҽ�����+�µ��ӶԸ���=3+ ![]() =4������ԭ���ӻ���ʽ��sp3 �� ������һ�Թ¶Ե��Ӷԣ����ӿռ乹��Ϊ�����Σ����Դ��ǣ������Σ�sp3��
=4������ԭ���ӻ���ʽ��sp3 �� ������һ�Թ¶Ե��Ӷԣ����ӿռ乹��Ϊ�����Σ����Դ��ǣ������Σ�sp3��
��4.��GaF3���۵����1000�棬GaCl3���۵�Ϊ77.9�棬��ԭ����GaF3Ϊ���Ӿ��壬GaCl3Ϊ���Ӿ��壬���Ӿ�����۵�ߣ����Դ��ǣ�GaF3Ϊ���Ӿ��壬GaCl3Ϊ���Ӿ��壬���Ӿ�����۵�ߣ�
��5.��GaAs���۵�Ϊ1238�棬�۵�ϸߣ��Թ��ۼ�����γ�����ԭ�Ӿ��壬�ܶ�Ϊ�� gcm��3 �� ���ݾ�̯�����㣬As�� ![]() ��Ga��4��1=4�����侧����ԭ����ռ�����V1=��
��Ga��4��1=4�����侧����ԭ����ռ�����V1=�� ![]() ����10��30 �� ���������V2=
����10��30 �� ���������V2= ![]() =
=  ����GaAs������ԭ�ӵ����ռ��������İٷ���Ϊ
����GaAs������ԭ�ӵ����ռ��������İٷ���Ϊ ![]() ��V1��V2�������ðٷ���=
��V1��V2�������ðٷ���= ![]() ��100%�����Դ��ǣ�ԭ�Ӿ��壻���ۣ�
��100%�����Դ��ǣ�ԭ�Ӿ��壻���ۣ� ![]() ��100%��
��100%��


 ���Ӣ��������ϵ�д�
���Ӣ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ������˵����ȷ���ǣ� ��
A.��״���£�22.4LCHCl3�к�����ԭ����ĿΪ3NA
B.���³�ѹ�£�2gD216O�к�������������������������ΪNA
C.�����£�0.1mol/LNa2CO3��Һ�У����������ӵ�����С��0.1NA
D.ͬ�¡�ͬѹ�£���ͬ��������������������ԭ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ڱ�����ʽ���ֶ�������ͼ������Ԫ�����ڱ���һ���֣��Ա���ѧ����Ԫ�����ڱ���˼������Ԫ�����ڱ��������ɣ��ش���������:
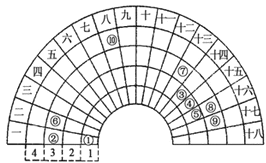
(1)д�����ڳ�ʽ���ڱ��е�λ��______________��
(2)Ԫ�آ͢ߵ�ԭ���������________��
(3)Ԫ�آڢݢ��γɵļ����Ӱ뾶��С�����˳����__________��
(4)Ԫ�آ٢ݿ����γɶ���10���Ӻ�18���ӵ����ӣ�д�����з�������Ҫ������ӵĵ���ʽΪ:4��18���ӵķ���________��10���ӵ�������__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����������仯�����������ȷ����
A.����������ˮ����˿�����ˮ���ռ�����
B.�����ڳ�������������Ӧ���ʲ����������Һ��
C.����������ˮ�������ݳ���������������
D.������������ȼ�ղ�������ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ȳ��һ����Ҫ���л�����ԭ�ϣ�����ȲΪԭ���ڲ�ͬ�ķ�Ӧ������
����ת�������»��������˵����ȷ����

A. ����������ķ���ʽΪC4H4������ȴ���������
B. ��Ϊƽ�������νṹ�������д���C��C��C==C����ʹ����KMnO4��Һ��ɫ
C. ����������Ȳ����ϩ����Ȳ��ȫȼ��ʱ�ĺ�������ͬ
D. ������ϩ�����Ľṹ������ʹ��ˮ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��ԭ��ص�װ��ͼ(![]() Ϊ������)����ش�
Ϊ������)����ش�
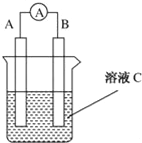
��1����CΪϡH2SO4��Һ��������ָ�뷢��ƫת��B�缫����ΪFe������������A�缫�Ϸ����ĵ缫��ӦʽΪ____________��
��2����CΪCuSO4��Һ��A�缫����ΪZn��B�缫����Ϊʯī��������ָ�뷢��ƫת����ʱBΪ______������Ӧһ��ʱ���B�缫���ܹ��۲쵽��������______________________��
��3����CΪNaOH��Һ��A�缫����ΪAl��B�缫����ΪMg�������Ϸ����ĵ缫��ʽΪ___________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪþ-�����������صĹ���ԭ��ʾ��ͼ����֪:��طŵ�ʱ����ת��Ϊ������þ�������������ת��Ϊ�䱽����������˵������ȷ����
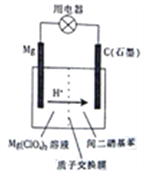
A. ��طŵ�ʱ��������þ�缫���������õ�������ʯī�缫
B. ��طŵ�ʱ��þ�缫�����ĵ������Һ��pH����
C. ��طŵ�ʱ��������ÿ����1mol�䱽��������12molH+ͨ�����ӽ���Ĥ
D. ��طŵ�ʱ��ʯī����Ϸ����ķ�ӦΪ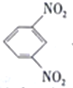 +12H+-12e-=
+12H+-12e-=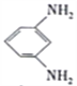 +4H2O
+4H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������õ���һ�ָ��ܵ�ة���п��أ����ڷŵ�ʱ�ĵ缫��ӦΪ��Zn+2OH����2e���TZnO+H2O��Ag2O+H2O+2e���T2Ag+2OH�� �� �ݴ��жϣ��������ǣ�������
A.������������
B.����������ԭ
C.����������ԭ
D.������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ϸ������ҪԪ����ռϸ�����ر��������ǣ� ��
A. ̼ B. �� C. �� D. ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com