
【题目】采用惰性电极,以去离子水和氧气为原料通过电解法制备双氧水的装置如下图所示。忽略温度变化的影响,下列说法错误的是

A.阳极反应为![]()
B.电解一段时间后,阳极室的pH未变
C.电解过程中,H+由a极区向b极区迁移
D.电解一段时间后,a极生成的O2与b极反应的O2等量
【答案】D
【解析】
a极析出氧气,氧元素的化合价升高,做电解池的阳极,b极通入氧气,生成过氧化氢,氧元素的化合价降低,被还原,做电解池的阴极。
A.依据分析a极是阳极,属于放氧生酸性型的电解,所以阳极的反应式是2H2O-4e-=4H++O2↑,故A正确,但不符合题意;
B.电解时阳极产生氢离子,氢离子是阳离子,通过质子交换膜移向阴极,所以电解一段时间后,阳极室的pH值不变,故B正确,但不符合题意;
C.有B的分析可知,C正确,但不符合题意;
D.电解时,阳极的反应为:2H2O-4e-=4H++O2↑,阴极的反应为:O2+2e-+2H+=H2O2,总反应为:O2+2H2O=2H2O2,要消耗氧气,即是a极生成的氧气小于b极消耗的氧气,故D错误,符合题意;
故选:D。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列说法正确的是
A.1mol的羟基与1mol的氢氧根离子所含电子数均为9NA
B.常温常压下,18g H2O含有的原子总数为3NA
C.标准状况下,11.2LCH3CH2OH中含有分子的数目为0.5NA
D.常温常压下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置进行的相应实验,能达到实验目的的是
A.利用图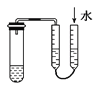 方法验证装置的气密性
方法验证装置的气密性
B.实验室里利用图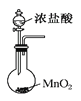 装置制备氯气
装置制备氯气
C.利用图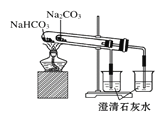 比较碳酸钠和碳酸氢钠的热稳定性
比较碳酸钠和碳酸氢钠的热稳定性
D.利用图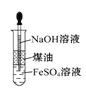 制备Fe(OH)2并能较长时间观察其颜色
制备Fe(OH)2并能较长时间观察其颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿(主要成分为二硫化亚铁铜:CuFeS2)是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。冶炼铜的反应为8CuFeS2+21O2 ![]() 8Cu+4FeO+2Fe2O3+16SO2 。
8Cu+4FeO+2Fe2O3+16SO2 。
(1)若CuFeS2中Fe的化合价为+2,反应中被还原的元素是__________(填元素符号)。
(2)用稀H2SO4浸泡上述反应制取铜后剩余的固体残渣,取少量所得溶液,检验溶液中存在Fe3+的方法是_________(注明试剂、现象、结论)。
(3)上述冶炼过程产生大量SO2。下列处理方案中合理的是_____________(填代号)
a 高空排放 b 用于制备硫酸 c 用纯碱溶液吸收制Na2SO3 d 用浓硫酸吸收
(4)验证黄铜矿冶炼铜的反应后气体中含有SO2的方法是________________。
(5)实验室制备,收集干燥的SO2,所需仪器如下。
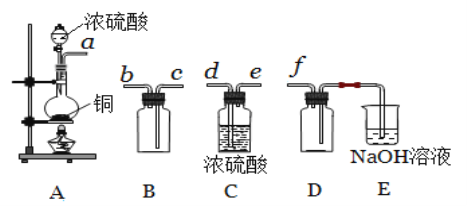
①其中装置A产生SO2 ,反应的化学方程式为_______________。
②请按气流方向连接各仪器接口,顺序为a →_____→_______→________→ _______→ f ,装置E中NaOH溶液的作用是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E是短周期中的5种非金属元素,它们的原子序数依次增大。A元素原子形成的离子核外电子数为零,C、D在元素周期表中处于相邻的位置,B原子的最外层电子数是内层电子数的2倍。E元素与D元素同主族; E的单质为黄色晶体,易溶于二硫化碳。
(1)请写出元素符号:
A_______,B_______,C_________,D_________,E__________。
(2)画出E的阴离子的结构示意图:__________
(3)A的单质和C的单质在一定条件下反应生成化合物X,该反应的化学方程式为_________。向X的水溶液中滴入酚酞溶液,会观察到_____________。
(4)将9g B单质在足量的D单质中燃烧,所得气体通入1L lmol/L NaOH溶液中,完全吸收后,溶液中大量存在的离子是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A.CaCO3与稀硝酸反应:![]()
B.FeSO4溶液与溴水反应:![]()
C.NaOH溶液与过量H2C2O4溶液反应:![]()
D.C6H5ONa溶液中通入少量CO2: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或有关化学用语的使用正确的是( )
A.在基态多电子原子中,p轨道电子的能量一定高于s轨道电子的能量
B.Fe原子的外围电子排布图为![]()
C.氧的电负性比氮大,故氧元素的第一电离能比氮元素的第一电离能大
D.铜原子的外围电子排布式为3d94s2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列物质中:①HCl、②N2、③NH3、④Na2O2、⑤C2H4、⑥NaOH、⑦Ar
(1)只存在极性键的分子是___;只由非极性键构成的非极性分子是__;(填序号,下同)。
(2)CO32﹣的中心原子的杂化轨道类型是__,微粒的空间构型是__。
(3)在K3[Fe(CN)6]中中心离子是__,配体是__,配位数是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com