
【题目】下列说法或有关化学用语的使用正确的是( )
A.在基态多电子原子中,p轨道电子的能量一定高于s轨道电子的能量
B.Fe原子的外围电子排布图为![]()
C.氧的电负性比氮大,故氧元素的第一电离能比氮元素的第一电离能大
D.铜原子的外围电子排布式为3d94s2
科目:高中化学 来源: 题型:
【题目】某研究小组以邻硝基甲苯为起始原料,按下列路线合成利尿药美托拉宗。
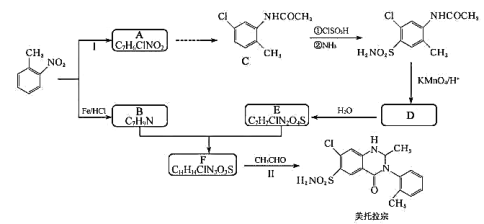
已知:
R-COOH+ 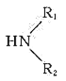
![]()
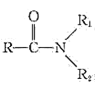
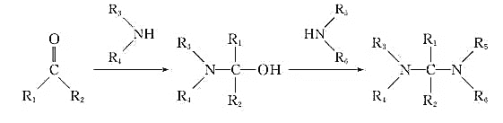
请回答:
(1)下列说法正确的是________。
A 反应Ⅰ的试剂和条件是![]() 和光照 B 化合物C能发生水解反应
和光照 B 化合物C能发生水解反应
C 反应Ⅱ涉及到加成反应、取代反应 D 美托拉宗的分子式是![]()
(2)写出化合物D的结构简式_________。
(3)写出![]() 的化学方程式____________。
的化学方程式____________。
(4)设计以A和乙烯为原料合成C的路线(用流程图表示,无机试剂任选)____。
(5)写出化合物A同时符合下列条件的同分异构体的结构简式_____。
![]() 谱和
谱和![]() 谱检测表明:①分子中共有4种氢原子,其中环上的有2种;②有碳氧双键,无氮氧键和
谱检测表明:①分子中共有4种氢原子,其中环上的有2种;②有碳氧双键,无氮氧键和![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】采用惰性电极,以去离子水和氧气为原料通过电解法制备双氧水的装置如下图所示。忽略温度变化的影响,下列说法错误的是

A.阳极反应为![]()
B.电解一段时间后,阳极室的pH未变
C.电解过程中,H+由a极区向b极区迁移
D.电解一段时间后,a极生成的O2与b极反应的O2等量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧是地壳中含量最多的元素,氮是空气中含量最多的元素。
(1)H2O中的O-H键、分子间的范德华力和氢键由强到弱的顺序依次为____>___>___。
(2)![]() 的沸点高于
的沸点高于 ,其原因是____。
,其原因是____。
(3)O、S、Se都属于第ⅤIA族元素,形成简单氢化物的沸点由高到低的顺序为____>____>____(填分子式)。
(4)如图1表示某种含氮有机化合物的结构简式,其分子内4个氮原子分别位于正四面体的4个顶点(见图2)。分子内存在空腔,能嵌入某种离子或分子并形成4个氢键予以识别。
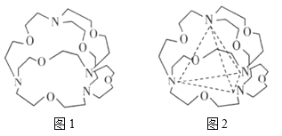
下列分子或离子中,能被该有机化合物识别的是____(填标号)。
A.CF4 B.NH4+ C.CH4 D.H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将NO2、NH3、O2混合气22.4L通过稀硫酸后,溶液质量增加了26.7g,气体体积缩小为4.48L。(气体体积均在标况下测定)剩余气体能使带火星的木条着火,则混合气体的平均相对分子质量为(4NO2+O2+2H2O=4HNO3)
A.28.1B.30.2C.33.1D.34.0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第四周期的Fe、Co、Ni、Cu、Zn等许多金属能形成配合物。
(1)NH3是一种很好的配体,氨气分子是____(填“极性”或“非极性”)分子,NH3的沸点____(填“高于”“等于”或“低于”)AsH3。
(2)科学家通过X-射线测得胆矾的结构示意图可简单表示如图所示:

图中虚线表示的作用力为__________。
(3)胆矾溶液与氨水在一定条件下可以生成Cu(NH3)4·SO4·H2O晶体。在Cu(NH3)4SO4·H2O晶体中,[Cu(NH3)4]2+为平面正方形结构,则呈正四面体结构的原子团是____,该原子团中心原子的杂化轨道类型是____。
(4)金属镍粉在CO气流中轻微加热,生成无色、有挥发性的液态Ni(CO)4,其分子呈正四面体构型。Ni(CO)4易溶于____(填字母)。
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然产物H具有抗肿瘤、镇痉等生物活性,可通过以下路线合成。

已知: (
(![]() 等)
等)
回答下列问题:
(1)A的链状同分异构体可发生银镜反应,写出这些同分异构体所有可能的结构:__________。
(2)在核磁共振氢谱中,化合物B有________组吸收峰。
(3)化合物X的结构简式为___________。
(4)D→E的反应类型为___________。
(5)F的分子式为_______,G所含官能团的名称为___________。
(6)化合物H含有手性碳原子的数目为_____,下列物质不能与H发生反应的是_______(填序号)。
a.CHCl3 b.NaOH溶液 c.酸性KMnO4溶液 d.金属Na
(7)以 和
和![]() 为原料,合成
为原料,合成![]() ,写出路线流程图(无机试剂和不超过2个碳的有机试剂任选)_______________。
,写出路线流程图(无机试剂和不超过2个碳的有机试剂任选)_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证Cl2、Fe3+、I2三者氧化性的相对强弱,某小组用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。
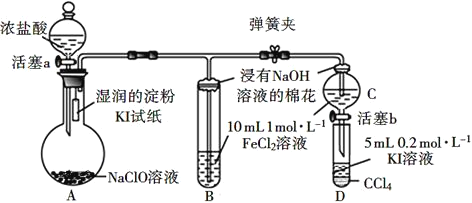
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.向B中加入一定量KSCN溶液,混合液显红色,一段时间后,B中溶液红色加深,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,写出A中发生反应的化学反应方程式:___。
(2)验证氯气的氧化性强于碘单质的实验现象是___。
(3)B中溶液发生反应的离子方程式是___。
(4)为验证Fe3+的氧化性强于碘单质,过程Ⅳ的操作和现象是___,对应反应的离子方程式是___。
(5)浸有氢氧化钠溶液的棉花作用是__。
(6)过程Ⅲ实验的目的是__。
(7)若将氯气通入无色碘化钾溶液中,无色溶液先变为黄色,继续通入氯气后,溶液又变为无色,已知每1molKI完全反应转移6mol电子,写出过量氯气与碘化钾溶液反应的离子方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种三电极电解水制氢的装置如图,三电极为催化电极a、催化电极b和Ni(OH)2电极。通过控制开关连接K1或K2,可交替得到H2和O2。下列说法错误的是( )
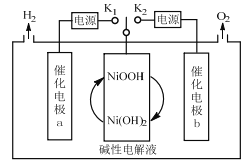
A.制O2时,电子由Ni(OH)2电极通过外电路流向催化电极b
B.制H2时,阳极的电极反应式为Ni(OH)2+OH--e-=NiOOH+H2O
C.催化电极b上,OH-发生氧化反应生成O2
D.该装置可在无隔膜的条件下制备高纯氢气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com