
【题目】氧是地壳中含量最多的元素,氮是空气中含量最多的元素。
(1)H2O中的O-H键、分子间的范德华力和氢键由强到弱的顺序依次为____>___>___。
(2)![]() 的沸点高于
的沸点高于 ,其原因是____。
,其原因是____。
(3)O、S、Se都属于第ⅤIA族元素,形成简单氢化物的沸点由高到低的顺序为____>____>____(填分子式)。
(4)如图1表示某种含氮有机化合物的结构简式,其分子内4个氮原子分别位于正四面体的4个顶点(见图2)。分子内存在空腔,能嵌入某种离子或分子并形成4个氢键予以识别。
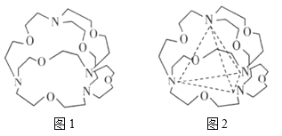
下列分子或离子中,能被该有机化合物识别的是____(填标号)。
A.CF4 B.NH4+ C.CH4 D.H2O
【答案】O-H键 氢键 分子间的范德华力 ![]() 形成分子内氢键,而
形成分子内氢键,而![]() 形成分子间氢键,分子间氢键使分子间作用力增大 H2O H2Se H2S B
形成分子间氢键,分子间氢键使分子间作用力增大 H2O H2Se H2S B
【解析】
(1)氢键键能介于化学键和分子间作用力之间,化学键键能最大,所以H2O分子内的O-H键、分子间的范德华力和氢键从强到弱依次为O-H键、氢键、范德华力;
(2)含分子间氢键的物质的沸点大于分子内氢键物质的沸点,![]() 形成分子内氢键,而
形成分子内氢键,而![]() 形成分子间氢键,分子间氢键使分子间作用力增大;
形成分子间氢键,分子间氢键使分子间作用力增大;
(3)O、S、Se同主族,其简单氢化物分别为H2O、H2S、H2Se,其中H2O分子之间存在氢键,氢键作用力大于范德华力,导致水的沸点异常的高,对于H2S和H2Se,则是范德华力主导,相对分子质量越高,沸点越高,因此沸点高低顺序为:H2O>H2Se>H2S;
(4)F、O、N电负性很大,与H元素形成的微粒之间可以形成氢键,正四面体顶点N原子与嵌入空腔的微粒形成4个氢键,该微粒应含有4个H原子,C元素不能形成氢键,所以选项中只有NH4+ 符合,故答案为B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】我国青海湖地区素有“夏天晒盐,冬天捞碱”之说。其中捞出的碱主要是碳酸钠和少量氯化钠的混合物。某同学以捞出的碱作为样品,并用下图装置对样品进行分析,根据量瓶中收集到的液体的体积来计算样品中碳酸钠的含量,下列装置中正确的是 ( )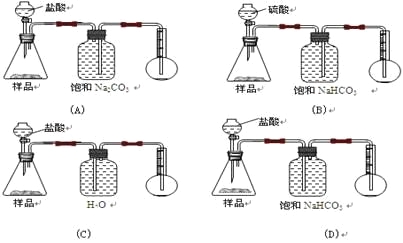
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置进行的相应实验,能达到实验目的的是
A.利用图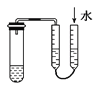 方法验证装置的气密性
方法验证装置的气密性
B.实验室里利用图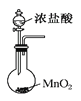 装置制备氯气
装置制备氯气
C.利用图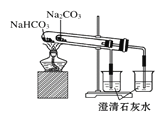 比较碳酸钠和碳酸氢钠的热稳定性
比较碳酸钠和碳酸氢钠的热稳定性
D.利用图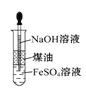 制备Fe(OH)2并能较长时间观察其颜色
制备Fe(OH)2并能较长时间观察其颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E是短周期中的5种非金属元素,它们的原子序数依次增大。A元素原子形成的离子核外电子数为零,C、D在元素周期表中处于相邻的位置,B原子的最外层电子数是内层电子数的2倍。E元素与D元素同主族; E的单质为黄色晶体,易溶于二硫化碳。
(1)请写出元素符号:
A_______,B_______,C_________,D_________,E__________。
(2)画出E的阴离子的结构示意图:__________
(3)A的单质和C的单质在一定条件下反应生成化合物X,该反应的化学方程式为_________。向X的水溶液中滴入酚酞溶液,会观察到_____________。
(4)将9g B单质在足量的D单质中燃烧,所得气体通入1L lmol/L NaOH溶液中,完全吸收后,溶液中大量存在的离子是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A.CaCO3与稀硝酸反应:![]()
B.FeSO4溶液与溴水反应:![]()
C.NaOH溶液与过量H2C2O4溶液反应:![]()
D.C6H5ONa溶液中通入少量CO2: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于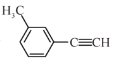 的说法正确的是
的说法正确的是
A.分子中有3种杂化轨道类型的碳原子
B.分子中共平面的原子数目最多为14
C.分子中的苯环由单双键交替组成
D.与Cl2发生取代反应生成两种产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或有关化学用语的使用正确的是( )
A.在基态多电子原子中,p轨道电子的能量一定高于s轨道电子的能量
B.Fe原子的外围电子排布图为![]()
C.氧的电负性比氮大,故氧元素的第一电离能比氮元素的第一电离能大
D.铜原子的外围电子排布式为3d94s2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)画出下列元素的原子结构示意图。
①核电荷数为13的元素:__________。
②某元素原子的最外层电子数等于次外层电子数:__________________ 。
③L 层电子数是M层电子数2倍的元素: ___________________ 。
④某同位素原子核内没有中子的元素: ___________________ 。
(2)写出1~18号元素中符合下列条件的原子(离子)的微粒符号和结构示意图。
①某元素原子L层上的电子数为K层的3倍: __________________ 。
②某元素原子L层上的电子数为K层的一半: _________________ 。
③得到2个电子后,电子总数与氩原子的电子总数相同的离子: ___________________ 。
④某元素原子的最外层电子数等于次外层电子数的2倍: ___________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2020年新冠肺炎疫情在全球多点爆发。新型冠状病毒对紫外线和热敏感,56℃持续30分钟、酒精、含氯消毒剂、过氧乙酸等均可有效灭活病毒。下列有关说法正确的是( )
A.84消毒液的有效成分是![]()
B.84消毒液与酒精混合使用可增强灭活病毒效果
C.加热能杀死病毒是因为蛋白质受热发生变性
D.聚丙烯树脂是生产无纺布口罩的初始原料之一,聚丙烯可以使酸性高锰酸钾溶液褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com